Onze cellen maken gebruik van allerlei eiwitten die als een pomp nuttige stoffen naar binnen transporteren. De motor van deze pompen draait op een stroom deeltjes, vaak natrium-ionen, zoals water een waterrad aandrijft. In Nature Communications publiceerden Groningse onderzoekers hoe dit transport door de celmembraan precies verloopt.
Het staat in alle leerboeken biologie: transport van buiten naar binnen (of omgekeerd) in cellen wordt aangedreven door een verschil in de concentratie van deeltjes in de cel en daarbuiten. Die deeltjes zijn meestal natrium- of kalium-ionen. Buiten de cel is de concentratie natrium-ionen doorgaans veel hoger dan in de cel, voor kalium geldt het omgekeerde. Maar hoe zorgt dat concentratieverschil nou precies voor de aandrijving? Dat wilden Dirk Slotboom, hoogleraar biochemie aan de Rijksuniversiteit Groningen en zijn team graag uitzoeken.
Kennislink publiceerde al eerder over het onderzoek van Slotboom naar transport over de celmembraan. “We weten bijvoorbeeld dat een transporteiwit, de pomp, drie natrium-ionen nodig heeft om een molecuul aspartaat, een belangrijke bouwsteen voor eiwitten, een cel in te krijgen. Maar hoe het transporteiwit dat precies voor elkaar krijgt heeft nog niemand kunnen ontdekken”, vertelt Slotboom. Duidelijk is wel dat op de een of andere manier natrium en aspartaat samen getransporteerd moeten worden. “Als natrium ook alleen de cel in kan, zou het concentratieverschil verdwijnen. En als aspartaat zonder natrium is te transporteren, zou het ook weer naar buiten kunnen gaan.”
Van leeg naar vol
Om het transportmechanisme te achterhalen moesten Slotboom en collega’s eerst de 3D of ruimtelijke structuur van het transporteiwit bepalen. En dan in twee varianten: met en zonder natrium en aspartaat. Dat is een langdurig proces, maar het leverde uiteindelijk een goed resultaat op. “We hadden dus twee punten in het proces, het lege en het volle transporteiwit. Met behulp van simulaties hebben we berekend wat de stappen daartussen zijn geweest.”
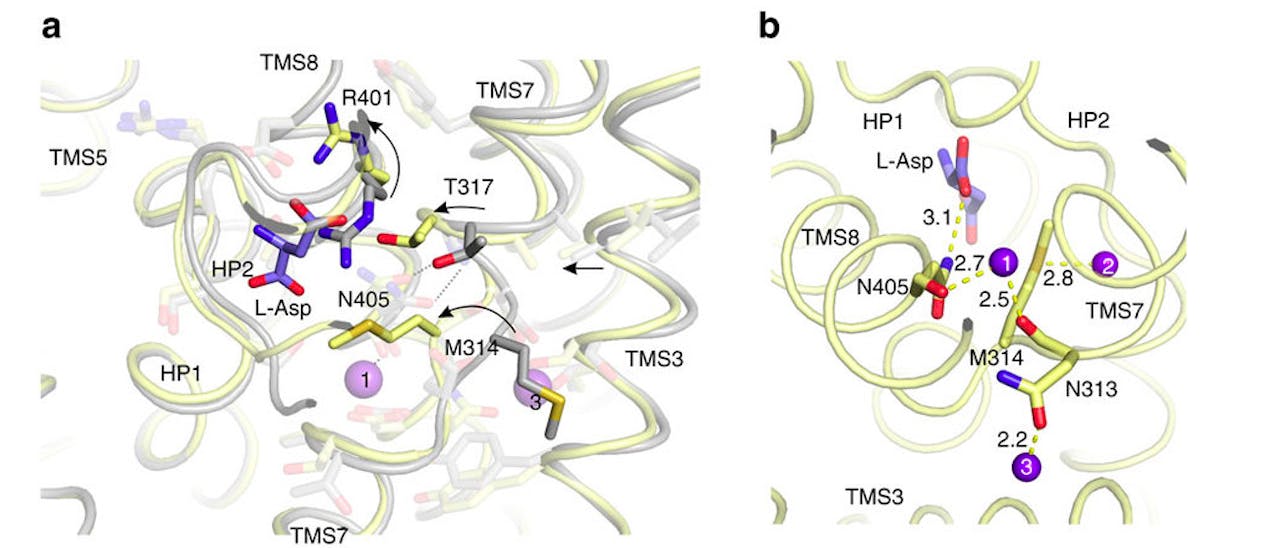
Uit die berekeningen kwam een mechanisme dat de werking verklaart. De lege vorm van het eiwit heeft helemaal niet de neiging om aspartaat te binden en ook de behoefte om een natrium-ion te binden is heel gering. Maar zodra er toch één natrium-ion aan vast gaat zitten, verandert de structuur en volgt een tweede natrium-ion. Daardoor verandert de structuur nog een keer en dan ontstaat een plek waar aspartaat zich heel erg thuis voelt. “En na de binding van aspartaat ontstaat een bindingsplek voor een derde natrium-ion”, legt Slotboom enthousiast uit.
Binnen- en buitendeur
Als dat derde natrium-ion vastzit aan het transporteiwit, vindt de laatste structuurverandering plaats. “Er gaat als het ware een dekseltje dicht, waarna het eiwit de deur naar buiten dicht doet, terwijl er een deur naar binnen open gaat.” Het derde natrium-ion is zeer zwak gebonden, dus het laat ook gemakkelijk los. Dit zorgt ervoor dat ook het aspartaat loslaat, net als de twee overgebleven natrium-ionen. Alles is nu in de cel gebracht. De binnendeur slaat dan dicht, waardoor de buitendeur opent gaat en het proces opnieuw kan beginnen.
Het is een elegant systeem, vindt Slotboom: “Alle stappen zijn nodig voor transport, aspartaat kan pas binden als er twee natrium-ionen aan het eiwit zitten, maar voor het daadwerkelijke transport is het derde ion nodig dat de deur dicht doet. En de zwakke binding van dat derde ion zorgt voor het loslaten van de lading.” Transporteiwitten komen voor in allerlei verschillende cellen en zijn uiterst belangrijk. Nauwkeurige kennis van het werkingsmechanisme kan dus helpen om bijvoorbeeld een cruciaal transport in schadelijke bacteriën plat te leggen.

