Hersencellen, hersenverbindingen of hersenactiviteit: welke scantechniek toont nou precies wat? En doen ze dit door foto’s en filmpjes van je brein te maken? Of juist door de elektriciteit van je hersencellen te meten? Of door deze zelfs te beïnvloeden? Dit naslagwerk is onderdeel van een serie over hersenspinsels over hersenscans: het bespreekt alle hersenscanstechnieken die in de serie aan bod komen.
Breinbeelden
MRI: een foto van je brein
Kernspintomografie, beter bekend als Magnetic Resonance Imaging (MRI), wordt gebruikt om gedetailleerde foto’s te maken waarop de structuur van de hersenen – de anatomie – goed te zien is. Op een MRI-beeld ziet de grijze stof (de cellichamen van de hersencellen) er bijvoorbeeld anders uit dan de witte stof (de uitlopers van hersencellen die de verbindingen tussen hersengebieden vormen) of hersenvloeistof.
Je zou de grijze stof kunnen zien als verschillende afdelingen van een ziekenhuis die met elkaar samenwerken, en de witte stof als de telefoonlijnen die deze afdelingen gebruiken om opdrachten aan elkaar over te brengen. Als elke afdeling goed zijn werk doet en als alle communicatie soepel gaat, functioneert het ziekenhuis optimaal. Of dit ook het geval is voor je brein, probeer je met een MRI-scan in kaart te brengen. Zo’n foto geeft namelijk informatie over de neurologische gezondheid van je hersenen. Anatomische structuren en afwijkingen, zoals tumoren zijn er bijvoorbeeld goed op te zien.
Zo’n MRI-foto kan ook gebruikt worden om te bepalen waar de hersenactiviteít zich bevindt. Die activiteit wordt dan gemeten met een aparte fMRI-scan. Van elke persoon die een fMRI-scan krijgt, wordt gelijk een anatomische MRI-scan gemaakt. Dit is belangrijk omdat geen enkel brein even groot is, en bij iedereen elke hersenstructuur net weer even iets anders gevormd is. Door deze persoonlijke anatomische MRI-scan naderhand op de gemeten hersenactiviteit (de fMRI-scan) te leggen, kan per persoon zo precies mogelijk worden ingeschat welke delen van de hersenen actief waren tijdens de fMRI-scans.
fMRI: kijken naar het brein in actie
Functionele Magnetische Resonantie Imaging (fMRI) maakt in plaats van een gedetailleerde foto een heus filmpje van de ‘hersenactiviteit’ terwijl de gescande persoon een taakje uitvoert. We spreken over ‘hersenactiviteit’, maar eigenlijk meet het fMRI-signaal het verschil tussen zuurstofrijk en zuurstofarm bloed in elk hersengebied.
De aanname is dat actieve hersencellen meer zuurstof nodig hebben en dat daarom het zuurstofgehalte van het bloed dat rondom actieve hersendelen stroomt, anders is dan rondom de minder actieve delen. Hier is bewijs voor, maar het blijft een aanname dat fMRI op deze wijze ook daadwerkelijk activiteit meet van de hersencellen. Het zuurstofgehalte verandert bijvoorbeeld veel trager dan de elektrische hersenactiviteit, en ook zitten bloedvaten niet precies op dezelfde plek als hersencellen.
MRI’s en fMRI’s worden dus met hetzelfde apparaat gemaakt, alleen met andere instellingen. In de hersenspinselserie zullen we omwille van de duidelijkheid echter wel ‘MRI-scanner’ of ‘fMRI-scanner’ gebruiken, zodat meteen duidelijk is welk type scan we bedoelen.
DTI: de communicatie-routes van je brein
Er is nog een derde manier om de MRI-scanner te gebruiken, die niet de hersengebieden of hun activiteit maar de verbindingen tussen de hersencellen meet. Dit zijn de telefoonlijnen waar we het in het begin over hadden.
Deze nieuwe techniek is nog tamelijk vers van de pers en heet diffusie-tensor imaging (DTI). Hierbij wordt de scanner zo ingesteld dat het MRI- signaal gevoelig is voor de verplaatsing – de diffusie – van watermoleculen. Watermoleculen zijn de deeltjes waaruit water is opgebouwd, en deze moleculen bevinden zich zo’n beetje overal in het brein. Als watermoleculen geen beperkingen om zich heen hebben, kunnen ze vrij rondbewegen. Maar binnen bepaalde structuren, zoals de verbindingen tussen de hersencellen, wordt die bewegingsvrijheid beperkt en stromen de moleculen vooral in een bepaalde oriëntatie: met de verbinding mee.
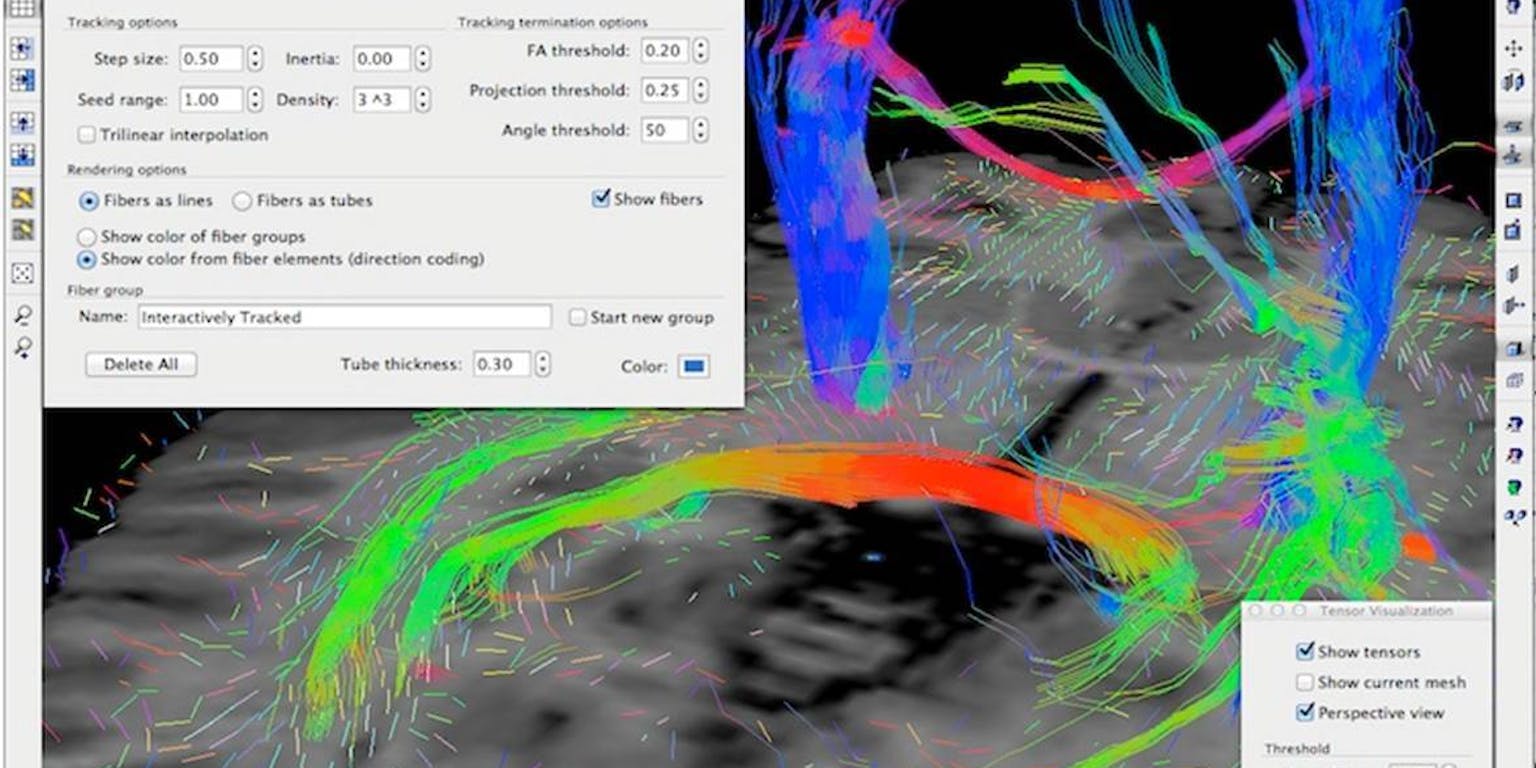
Op een DTI-scan zie je deze oriëntatie van de verplaatsing, en daarmee ook gelijk de zenuwbanen die worden gevormd door de uitlopers van hersencellen – de axonen. Vaak lopen er bundels van (honderden) miljoenen van het ene naar het andere hersengebied. DTI maakt beelden van de oriëntatie en de dikte van deze zenuwbundels, en laat hiermee zien welke hersengebieden met elkaar communiceren.
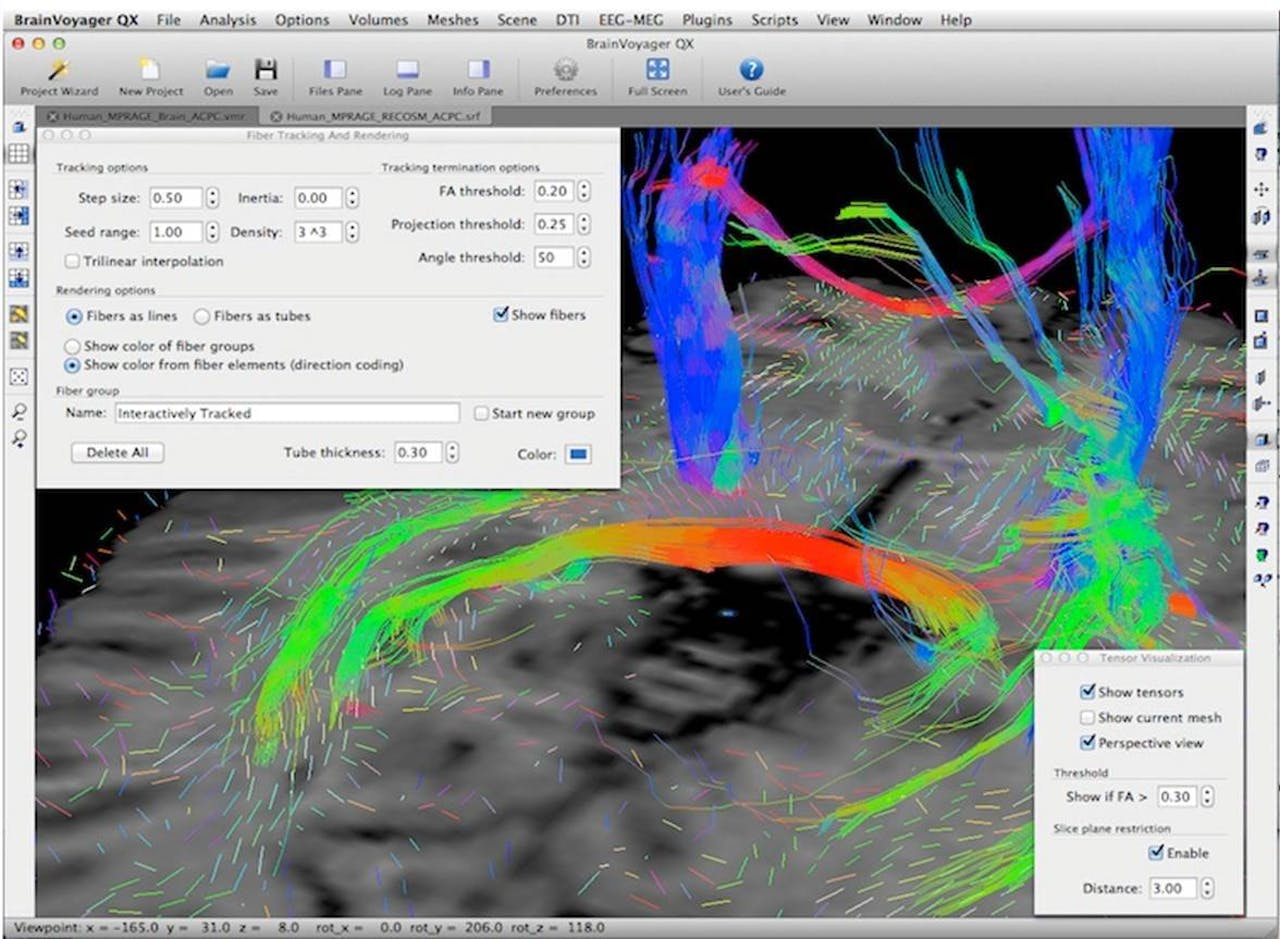
De dikke blauwe bundel op de foto – de tractus corticospinalis – loopt in beide hersenhelften helemaal verticaal: van het topje van je hoofd naar je ruggemerg, en zorgt ervoor dat je je bewegingen kan coördineren en uitvoeren. Het feloranje/-rode deel van de dikke bundel in het midden loopt juist helemaal horizontaal: dit is het corpus callosum – ook wel de hersenbalk genoemd – die er met zijn 200 miljoen axonen voor zorgt dat je hersenhelften met elkaar kunnen communiceren.
Breingolven
EEG: de elektriciteit van je brein
Bij het meten van een elektro-encefalogram (EEG) worden aan de buitenkant van het hoofd, met behulp van elektroden in een soort badmuts, elektrische signalen vanuit het brein opgevangen. Communicatie tussen hersencellen verloopt namelijk onder andere door middel van elektriciteit: als een hersencel ‘geactiveerd’ wordt, loopt er als het ware een stroompje door de cel.
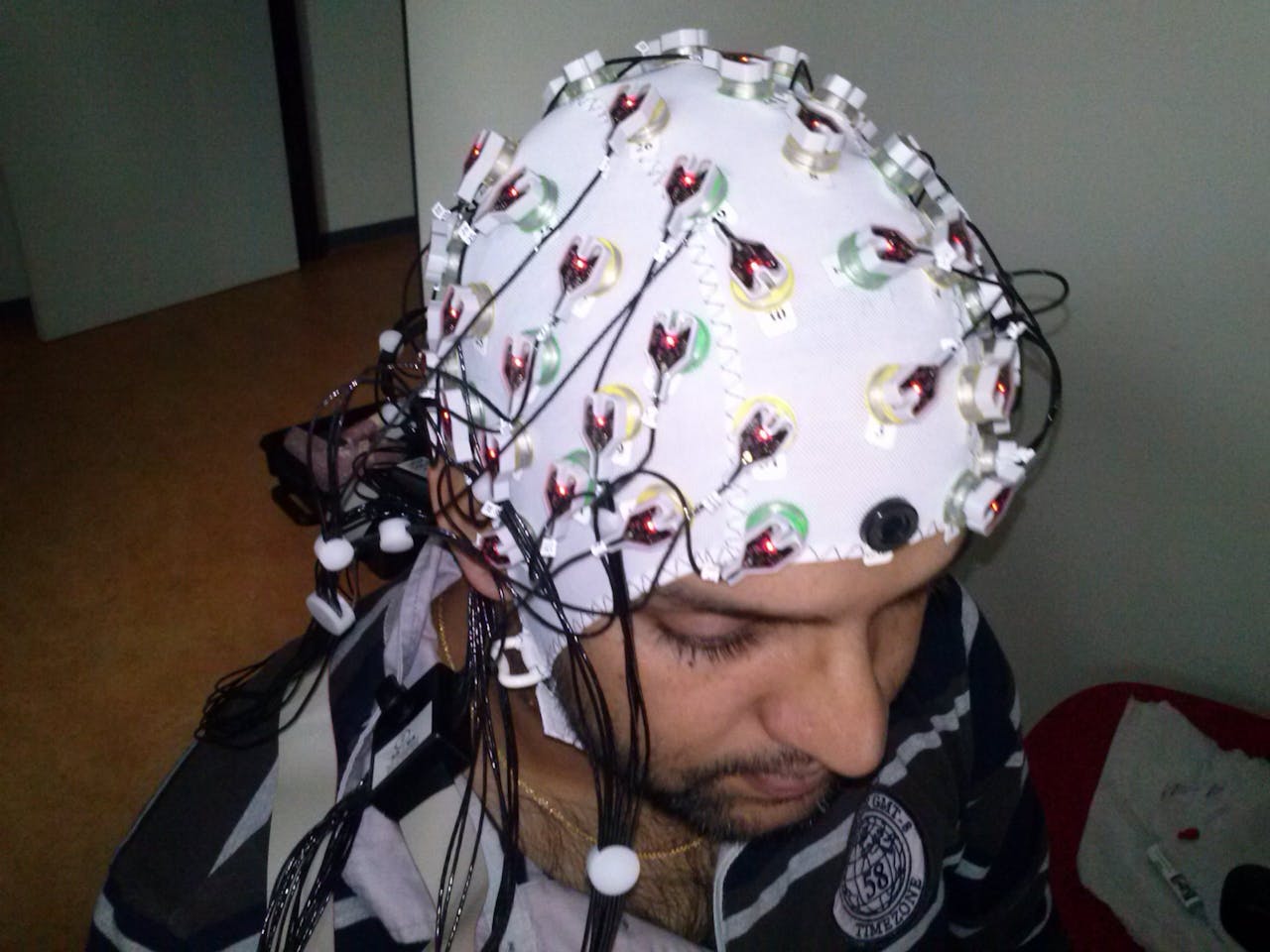
De EEG-muts
Nienke van AtteveldtAfhankelijk van de sterkte en aard van dit signaal wordt het stroompje wel of niet doorgegeven aan andere hersencellen. Als een groep hersencellen dezelfde soort elektrische activiteit vertoont, en als deze cellen dezelfde oriëntatie hebben, dan is het totale signaal dat geproduceerd wordt sterk genoeg om aan de buitenkant van de schedel te worden opgevangen. De elektrische signalen die op deze manier gemeten worden, zijn dus altijd de som van de elektrische activiteit van duizenden tot miljoenen hersencellen.

Omdat we het EEG aan de buitenkant meten, weten we niet precies waar in het brein het signaal is ontstaan. Dit komt onder andere omdat de signalen van verschillende groepjes hersencellen met elkaar worden vermengd. Als het gebied waar je als onderzoeker geïnteresseerd in bent, wat dieper in het brein ligt, zal het elektrische signaal eerst door andere actieve delen van het brein heen gaan voordat het de schedel bereikt.
Vervolgens wordt het signaal nogmaals vervormd en verspreid zodra het de schedel passeert. Hoe dieper een groep cellen ligt, hoe sterker het signaal vervormd zal zijn. De meetlocatie op de schedel zegt dus niet direct iets over waar het signaal is ontstaan in de hersenen. Dit is een nadeel van EEG. Zeker ten opzichte van fMRI, dat echte 3-dimensionale beelden maakt. Een groot voordeel van EEG is dat de signalen zeer nauwkeurig zijn in tijd. Dit is bij fMRI niet het geval, omdat het niet de hersenactiviteit zelf, maar – zoals hierboven uitgelegd – de langzamere veranderingen in bloedsamenstelling meet.
MEG:de magnetische velden van je brein
Magneto-encefalografie (MEG) maakt ook gebruik van een soort elektroden, maar deze meten niet de elektrische activiteit zelf, maar de veranderingen in magnetische velden als gevolg van de elektrische activiteit van hersencellen.
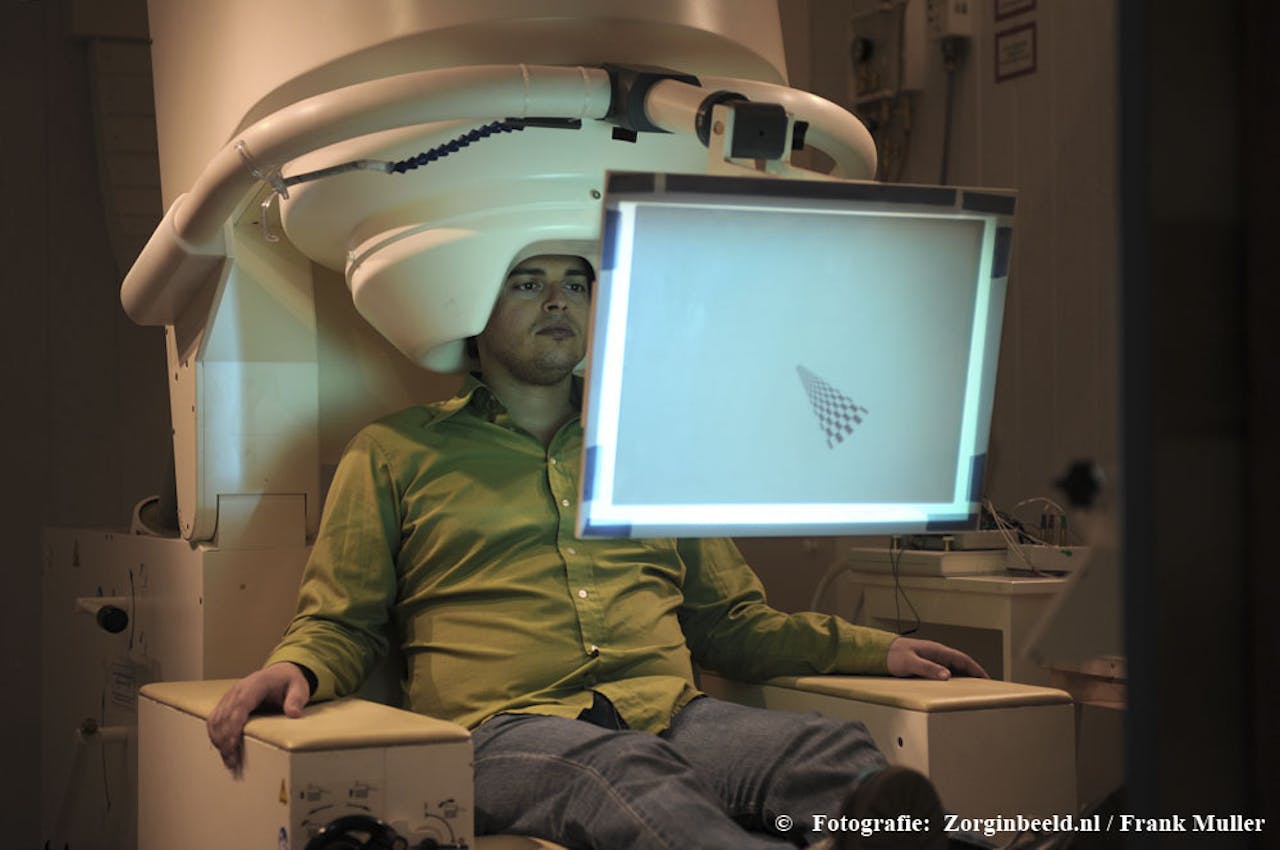
Een taakje uitvoeren, terwijl je onder de ‘MEG-droogkap’ zit
Donders Instituut NijmegenHet magnetische signaal wordt gemeten met behulp van sensoren in een soort enorme droogkap die over het hoofd wordt geplaatst. Doordat het MEG net een ander aspect meet van de hersenactiviteit, is het voor bepaalde factoren gevoeliger dan het EEG.
Een voordeel van MEG boven EEG is dat het magnetisch signaal minder sterk vervormd wordt door de tussenliggende hersengebieden en de schedel, waardoor het duidelijker is waar het signaal vandaan komt. Het MEG kan op eenzelfde manier gebruikt worden voor onderzoek als ERP: het signaal als reactie op een prikkel wordt dan gemiddeld tot een event-related field (ERF).
Breinstimulatie
TMS: je brein elektrisch ‘ontregelen’
Transcraniële Magnetische Stimulatie (TMS) wordt in tegenstelling tot de bovenstaande technieken niet gebruikt om activiteit van het brein te meten, maar juist om de activiteit in bepaalde hersengebieden te stimuleren of te ontregelen. Veranderingen in gedrag na het opwekken of afzwakken van de activiteit in een bepaald gebied zeggen veel over de mogelijke functie van dat hersengebied.
Bij TMS houdt men een spoel van koperdraad boven het hoofd van de proefpersoon of patiënt. Door de spoel loopt een sterke elektrische stroom die een magneetveld genereert dat door de schedel heendringt. Die magneetpuls induceert een elektrisch stroompje in het brein dat de hersencellen stimuleert. Zo kun je een bepaald gebied stimuleren of juist afzwakken, en vervolgens de reactie van de proefpersoon op deze ontregeling meten. Dit is vaak een gek gezicht: het stimuleren van een gedeelte van de motorische schors kan bijvoorbeeld leiden tot het bewegen van een vinger, zonder dat de proefpersoon dit zelf wil!

Als je zo’n magneetpuls gedurende enkele minuten achter elkaar herhaaldelijk toedient (repetitive TMS of rTMS), dan zet je het gestimuleerde gebied een tijdje ‘uit’. Op die manier kun je doen alsof een proefpersoon een beschadiging in het betreffende gebied heeft en kijken wat het effect daarvan is. Dat is heel handig, want in vroeger tijden moesten hersenonderzoekers soms jarenlang wachten tot er een patiënt was met een aandoening in precies dat gebied waarin zij geïnteresseerd waren.
Een groot voordeel van TMS boven andere technieken is dat je met de juiste timing van de magneetpuls binnen een taak iets te weten kunt komen over de volgorde waarin hersengebieden bepaalde informatie verwerken. Een nadeel is dat niet elk hersengebied even goed bereikt kan worden met TMS. Ook merkt de proefpersoon er meer van dan van EEG of fMRI, TMS behoort dan ook tot de zogenoemde invasieve technieken: ze dringen het brein binnen en veranderen signalen, in plaats van dat ze alleen bestaande signalen meten.
Diepe hersenstimulatie: een pacemaker voor je brein
Diepehersenstimulatie (DHS) is een nieuwe en experimentele techniek waarbij elektrodes tijdens een hersenoperatie diep in het brein worden ingebracht. Door middel van een stimulator met een batterij (een soort pacemaker) kunnen via de elektrode stroomstootjes naar bepaalde hersengebieden worden gestuurd. De techniek is dus net als TMS invasief.
Dit klinkt misschien een beetje griezelig, zo’n elektrode in je hersenpan, maar veel mensen met de ziekte van Parkinson hebben er baat bij. Als de elektrode op de juiste plek zit, stopt de elektrische puls de ernstige trillingen – de zogeheten tremoren – waar de patiënt last van heeft direct, en ontspant de vastzittende spieren. De stimulator wordt netjes onder de huid van de buik weggewerkt en kan met behulp van een afstandsbediening aan en uit worden gezet. In het TEDx -filmpje hieronder laat de Amerikaanse neuroloog Andres Lozano zien hoe Parkinsonpatiënten met een soort afstandsbediening zelf de elektrode in hun hersenen aanzetten, en zo vanaf het ene op het andere moment hun spastische bewegingen stoppen.
http://www.youtube.com/watch?v=gZCgWmose3c
Bij de ziekte van Parkinson is DHS bewezen effectief. Men onderzoekt nu of DHS ook zin heeft bij de behandeling van zware depressies en andere ernstige psychiatrische aandoeningen, zoals een Obsessief Compulsieve Stoornis (OCD). Ook al zijn daarvan ondertussen meerdere succesverhalen bekend, het blijft voor de neurochirurg een lastige klus om te bepalen waar de elektrodes precies aangebracht moeten worden. Als je één enkel hersengebied probeert te stimuleren, beïnvloedt dat een heel netwerk van hersengebieden.
Daarom wordt er tijdens de operatie gebruik gemaakt van functionele en structurele MRI-beelden om de elektrode heel nauwkeurig te plaatsen. En natuurlijk ook om te kijken of de elektrode tijdens het inbrengen geen andere vitale onderdelen, zoals bloedvaten raakt. Tijdens de operatie blijft de patiënt bij bewustzijn, zodat de chirurg door middel van gerichte vragen kan bepalen wat het effect van zijn handelingen is. Dit kan gewoon bij breinoperaties: hersencellen hebben geen receptoren voor pijn, waardoor de patient geen last heeft van al dat snijwerk. Desondanks weet je nooit precies hoe ver het effect van de stimulatie zal reiken en welke minder gewenste veranderingen dat mogelijk teweegbrengt.