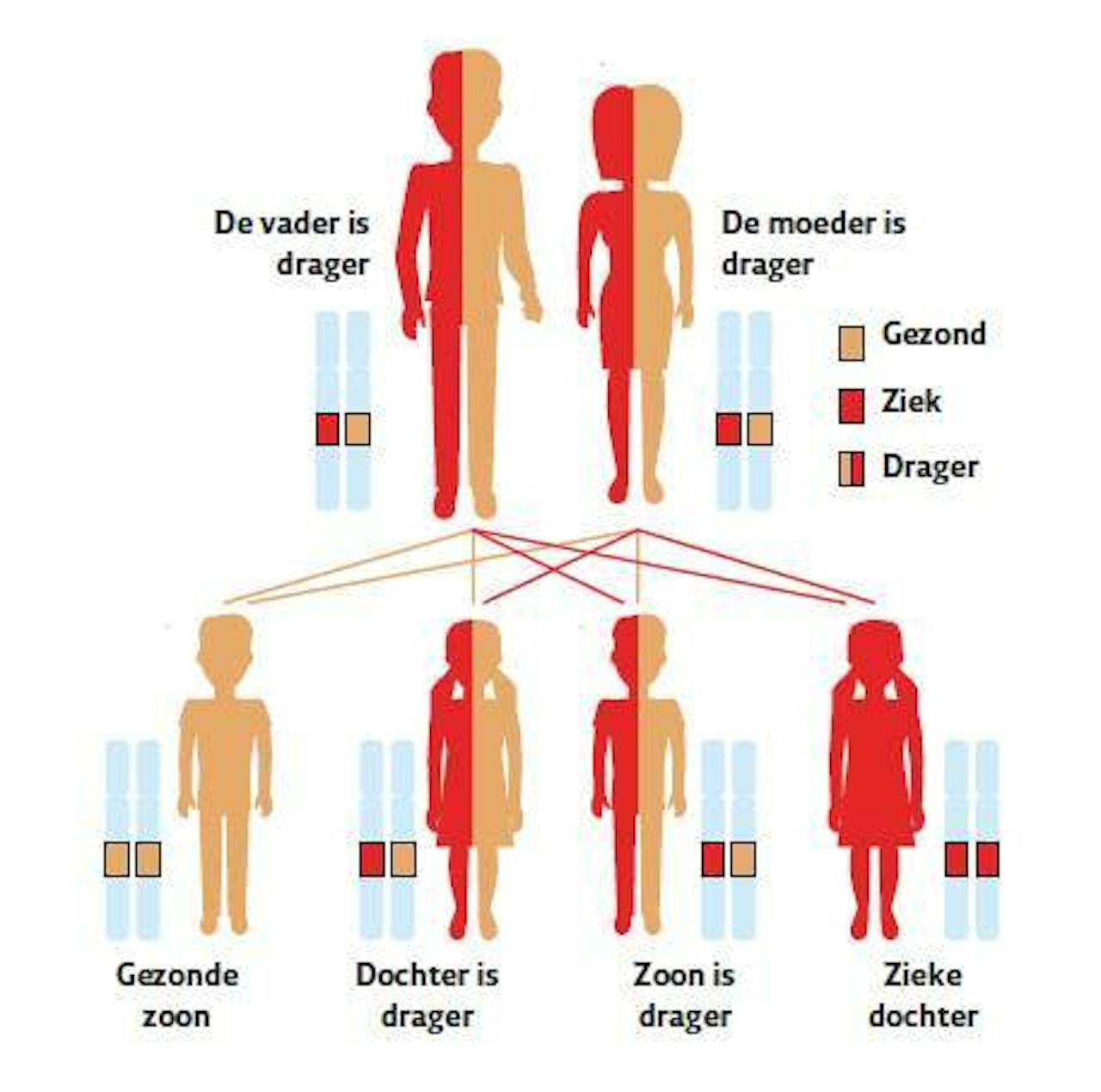
Een baby zonder ernstige erfelijke afwijkingen. Welke ouders willen dat nou niet? Sinds vorig jaar kunnen Nederlandse en Belgische ouders hun DNA op tientallen ziektes laten testen. Nog voordat het kind in de baarmoeder zit.
Net zwanger en al meteen de keuze: doe ik een combinatietest of niet? Deze test wordt in Nederland tussen de 11e en 14e week van de zwangerschap aangeboden en bekijkt of er een verhoogde kans is dat het kind downsyndroom, het syndroom van Edwards of het syndroom van Patau heeft. De combinatietest is een kansberekening en bestaat uit twee onderzoeken: een bloedonderzoek naar enkele eiwitwaarden en een nekplooimeting bij het ongeboren kind met behulp van een echo. Ook de leeftijd van de moeder speelt een rol in de bepaling van de kans op een baby met een van de drie syndromen.
Mijn uitslag was goed. De kans op downsyndroom was 1:6500, op Edwards 1:56.000 en op Patau 1:100.000. Ik hoefde gelukkig niet af te wegen of en welk vervolgonderzoek (vruchtwaterpunctie of vlokkentest) ik wilde. Toch was ik niet meteen opgelucht, want wat zegt mijn uitslag nou? De test kan er ook naast zitten. De combinatietest ontdekt tachtig van de honderd kinderen met downsyndroom. Mijn kans is 1:6500. Van de 65.000 zwangeren dragen er dus tien een kind met Down. Van die tien worden er acht wel ontdekt door de test en twee niet. De kans dat ik een kindje draag dat Down heeft – ondanks mijn gunstige testuitslag – is 2 op de 65.000, ofwel 1:37.500. Met die onzekerheid kan ik leven. Vanaf 1 april 2017 zal de onzekerheid iets minder worden, want dan mogen alle stellen in Nederland de veel betrouwbaardere NIPT-test in plaats van de combinatietest laten doen.
Wat dat betreft hadden mijn ouders het maar makkelijk. Er waren geen echo’s en tests. De vruchtwaterpunctie of vlokkentest werden alleen boven de 36 jaar aangeboden. Je wist niet of je een zoon of dochter zou krijgen en niet wat de precieze uitgerekende datum was. En dus ook niet of hij of zij gezond was. Gelukkig zijn de meeste baby’s dat wel. 95 tot 97 procent van de kinderen komt gezond ter wereld. Eigenlijk gaf het feit dat je gewoon af moest wachten veel rust, zegt mijn moeder.
Screenen voor het kind gemaakt is
Toch neemt het aantal tests en controles toe. Sinds vorig jaar is het in twee Nederlandse ziekenhuizen voor ouders met een kinderwens zelfs mogelijk om hun DNA al vóór de bevruchting te laten testen. Zo’n tien stellen per maand komen er voor naar het Academisch Medisch Centrum (AMC) in Amsterdam. Daar wordt hun DNA uitgeplozen en onderzocht op het dragen van vijftig ernstige erfelijke ziekten. Dit zijn veelal aandoeningen die op kinderleeftijd beginnen, ernstig lijden en vaak een vroege dood veroorzaken.
Door de test te doen, willen de stellen een eventuele verhoogde kans op een van de ziektes bij hun toekomstige kind achterhalen. Na de uitslag hebben zij verschillende mogelijkheden om de geboorte van een ziek kind te voorkomen. De test is niet goedkoop: 650 euro per persoon. Er is nog geen zorgverzekeraar die hem vergoedt, behalve voor mensen met een verhoogd risico op een specifieke ziekte. In het UMC Groningen wordt gratis getest, maar alleen binnen wetenschappelijk onderzoek dat voorlopig voldoende proefpersonen heeft.

In dat Groningse onderzoek bekijken wetenschappers hoe toekomstige ouders het vinden om zo’n test aangeboden te krijgen, hoe ze de test ervaren als ze meedoen, of ze echt begrijpen waaraan ze meedoen en of het mogelijk is dat huisartsen de test in de toekomst aan gaan bieden. In 2016 kregen vierduizend 18 tot 40-jarige vrouwen van hun huisarts de vraag of ze in aanmerking kwamen voor de test en of ze mee wilden doen. Er reageerden achthonderd vrouwen. Zestig procent bleek buiten de doelgroep te vallen (ze hadden bijvoorbeeld geen kinderwens, geen partner, of waren zwanger). “Uiteindelijk namen 180 stellen deel aan het onderzoek”, zegt UMCG-hoogleraar klinische genetica Irene van Langen.
Ook de Amsterdamse deelnemers krijgen het verzoek mee te werken aan wetenschappelijk onderzoek. 95 procent doet dat ook. De vragen dienen om erachter te komen wat de motivatie is voor mensen om mee te doen en wat de impact van de test is. “Een van de redenen is bijvoorbeeld dat een stel al een kindje met een ernstige aandoening heeft en dat niet nog een keer mee wil maken”, zegt klinisch geneticus Phillis Lakeman van het AMC.
Commerciële test
Belgische koppels kunnen terecht bij het bedrijf Gendia in Antwerpen. Dat bedrijf biedt voor 390 euro de Amerikaanse Counsyl-test aan die de kans op 104 ziektes bekijkt. De Groningse, Amsterdamse en Belgische test vertonen overeenkomsten, maar kijken ook allemaal naar andere ziektes. De ziektes uit de Groningse test zijn het scherpst gedefinieerd: ernstige, onbehandelbare, recessieve ziekten (zie kader) die direct na de geboorte of bij jongere kinderen beginnen.
De Amsterdamse test bevat ook een aantal iets mildere ziekten. Lakeman: “Dat komt omdat de test voortkomt uit de samenvoeging van verschillende dragerschapstesten voor ziekten die bij sommige bevolkingsgroepen relatief vaak voorkomen.” Zo is een op de zeven Surinamers drager van het gen voor sikkelcelanemie. “Op die tests kregen we positieve reacties. En ondertussen was de techniek zover dat we meerdere ziektes tegelijkertijd konden testen.” De nieuwe test is een uitgebreide versie van de oude tests die werden aangeboden, aangevuld met ernstige, recessieve ziekten waarmee in Nederland jaarlijks een oftwee kinderen worden geboren.
Dragerschapstesten maken het mogelijk al te screenen op ziektes voordat het kind gemaakt is.
Wikimedia Commons via CC BY 2.0De Nederlandse onderzoekers zijn niet erg te spreken over de commerciële tests die onder andere door de Zuiderburen worden aangeboden. Het was een van de redenen om in Nederland een test via een academisch ziekenhuis beschikbaar te maken. “De Antwerpse Gendia-test bestaat uit een mix van ernstige en milde ziekten, ziektes die meteen na de geboorte beginnen en ziektes die veel later ontstaan. Dat maakt de voorlichting erover lastig”, zegt Lakeman. “Zo zitten er aandoeningen bij waarvan je niet weet of je kind ze ooit gaat krijgen, ook al erft het kind van beide ouders het gemuteerde gen”, zegt Van Langen. “Dat schept alleen maar verwarring.” Lakeman: “De test kijkt bovendien alleen naar de bekende mutaties op een gen, dus niet naar het hele gen. Ook is de test niet specifiek voor mutaties die bij Belgische of Nederlandse families voorkomen. Zo zitten er mutaties bij die alleen bij Finse populaties voorkomen.”
Momenteel is er nog geen academisch ziekenhuis in België dat een uitgebreide dragerschapstest aanbiedt, maar die plannen zijn er wel. “In een academische setting kunnen stellen op de juiste manier begeleid worden en counseling krijgen”, zegt De Sutter. “Dit soort tests vereisen een goede uitleg en die ontbreekt bij commerciële tests.”
Ziektekeuzes
Er zijn honderden recessief erfelijke ziekten. Eén ziekte kan door een fout in verschillende genen ontstaan en de fout kan op verschillende plekken in het gen ontstaan. De ernst van de ziekte kan per locatie verschillen. En dan zijn er nog foutjes die helemaal niks veranderen aan iemands gezondheid. Hoe maak je de keuze voor de ziektes in de test en hoe bepaal je iemands uiteindelijke ziektekans?
“De huidige Groningse test is tot stand gekomen door veel gesprekken met verschillende specialisten”, zegt Van Langen. “Naast dat het om onbehandelbare, recessieve ziektes moest gaan die op jonge leeftijd beginnen, moest de totale kans op dragerschap voor een stel relatief hoog zijn (gemiddeld 1 op 150).” De Sutter zou graag zien dat een toekomstige Belgische test aan dezelfde voorwaarden voldoet. “Ik denk dat het goed is hierin het Nederlandse voorbeeld te volgen.” Buiten de gekozen vijftig aandoeningen, zijn er nog veel meer ziektes die aan de opgestelde voorwaarden voldoen. “Er komt zeker een nieuwe, uitgebreide, versie”, zegt Lakeman. “We zijn al door diverse specialisten benaderd met het verzoek bepaalde aandoeningen op te nemen.”
De makers van zowel de Groningse als de Amsterdamse test, schatten dat 1 op de 150 koppels drager is van dezelfde recessieve ziekte. Aangezien een kind van zo’n koppel een kans van 1 op 4 heeft de ziekte te krijgen (zie kader), is de kans dat een toekomstig kind een willekeurige ziekte uit de test zal hebben, 1 op 600. “Dat is hoger dan de kans van een gemiddelde vrouw op het dragen van een kind met het syndroom van Patau, Edwards of Down”, zegt Lakeman. “Bovendien zijn de ziektes in onze test veel ernstiger”, voegt Van Langen toe. Toch komt de NIPT nu voor iedereen beschikbaar in Nederland en is deze dat al in België. “Voordat wij gesprekken met zorgverzekeraars over vergoeding van onze test kunnen voeren, wil de politiek eerst de resultaten van het onderzoek afwachten”, zegt Lakeman.

Testen of niet. De kans op een gezond kind is gelukkig vele malen groter dan de kans op een ziek kind.
Flickr.com, Daniel via CC BY-NC-ND 2.0Embryo’s testen
Mocht een stel positief getest worden als drager voor dezelfde ziekte, dan krijgt het een gesprek met een klinisch geneticus. Op basis van die uitslag kunnen de aanstaande ouders besluiten dat ze afzien van kinderen. Of de vrouw wordt zwanger en ze besluiten het ongeboren kind specifiek op die ziekte te laten onderzoeken. Vervolgens kunnen ze besluiten over te gaan op abortus of zich voor te bereiden op de komst van een ziek kind. Of ze kiezen voor een zaad- of eiceldonor. Een andere optie is om te kiezen voor ivf en de embryo’s al in het lab te laten onderzoeken op de ziekte. Voor alle ziektes uit de Nederlandse testen is dat al mogelijk. Daarbij wordt alleen een embryo zonder de ziekte teruggeplaatst. “We bekijken momenteel of we in de toekomst de dragerschapstest standaard aan stellen in een ivf-traject aan kunnen bieden”, zegt Van Langen.
Maar zelfs al kiest een stel voor ivf met embryoselectie, dan weten ze nog niet of hun kind gezond is. Alleen dat het niet een van de vijftig erfelijke ziektes uit de test heeft. Tijdens de zwangerschap komen ze voor de keuze van de NIPT of de combinatietest te staan en bij 20 weken volgt de echo waarbij gekeken wordt of het kind geen lichamelijke afwijkingen als een open ruggetje, open schedel, hartafwijkingen of een gat in de buikwand heeft. En als het kind eenmaal geboren is volgt de hielprik, die het bloed van de pasgeborene op een kleine twintig erfelijke, behandelbare, aandoeningen onderzoekt.
Veel om over na te denken dus. Voorlopig kan ik alleen maar hopen dat ik straks een gezond kind op de wereld zet. En gelukkig is de kans daarop vele malen groter dan de kans op een ziek kind.