Jarenlang wilde ik zelfstandig onderzoeker worden. Ik was er bijna. Maar toen kwam COVID waardoor ik abrupt op verlof moest en mijn essentiële experimenten niet kon afmaken. Dag plannen! Dag toekomst als zelfstandig onderzoeker. Maar dit opende wel nieuwe deuren: Hallo klinisch onderzoek!
Eindelijk was daar het moment voor mij: ik kon mijn persoonlijke beursaanvraag indienen. Ik hoefde alleen nog maar een paar essentiële experimenten te doen (ter bevestiging van mijn pilot data). Maar aangezien ik cardiovasculaire veroudering bestudeer (de veroudering van het hart en bloedvaten), lieten deze laatste essentiële experimenten behoorlijk op zich wachten. De muizen voor mijn onderzoek moesten namelijk een leeftijd van minimaal 19 maanden hebben.

De muizen voor mijn onderzoek moesten minimaal 19 maanden oud zijn.
Pixabay CC0En gelukkig was dit in maart/april 2020 eindelijk het geval! Ik had de experimenten tot in detail gepland, alle benodigde labmaterialen besteld en alle experimenten van tevoren getest. Kortom, alles zou perfect samenkomen. Ik zou de versuikering (glycosylatie) van specifieke eiwitten in de ruimte tussen de cellen van de bloedvaten (extracellulaire matrix) en van de eiwitten op de celmembraan van cellen van ons afweersysteem vergelijken tussen jonge en oude muizen met de hulp van Mass Spectometry.
Dit is een techniek die door het beschieten van eiwitten met electronen, kleinere stukjes eiwit creëert met een heel specifieke massa en lading (mass/ charge). Hierdoor kunnen we exact herleiden van welk eiwit dit fragment afkomstig is en of dit stukje eiwit versuikerd is. Deze versuikering is belangrijk voor de functie van een eiwit in de ontwikkeling van een ziekte. Een verschil in glycosylatie van eiwitten kan mogelijk bijdragen aan de veroudering van bloedvaten.
/a>
Dit hoopte ik te bevestigen in de cellen die ik zou isoleren uit de bloedvaten van oude en jonge muizen. Hiermee kon ik het belang aantonen voor mijn vervolgonderzoek naar glycosylatie van eiwitten in de extracellulaire matrix in cardiovasculaire veroudering. DE beursaanvraag voor mijn opstap naar zelfstandig onderzoeker!
Maar toen gebeurde het…De pandemie.
De pandemie die alle postdocs in ons lab plots op verlof zette; betaald worden door de overheid om niet te werken. Voor 4-5 maanden. Mijn experimenten mochten dus NIET worden uitgevoerd. Mijn plan werd hiermee behoorlijk overhoop gegooid. Hoe moest dat nu met mijn beursaanvraag?
Zelfstandig onderzoeker, dat was wat ik altijd graag wilde worden. Ik wilde mijn nieuwsgierigheid volgen, creatief bezig zijn en integer werken zonder me direct te laten inbinden door publicatiedruk. Het schrijven van mijn eigen beurs en krijgen van mijn eigen geld was dan ook al die tijd mijn doel. Daarmee krijg je als wetenschapper namelijk de vrijheid om jouw onderzoek uit te voeren.
Maar COVID veranderde dit plan compleet. Door COVID en BREXIT werd het vrijwel onmogelijk voor me om mijn beursaanvraag te schrijven. Zonder het uitvoeren van de laatste essentiële experimenten was de beursaanvraag niet robuust genoeg. Het ging me dus niet lukken. Ook al liep mijn contract pas af in april 2021, het was onmogelijk om voor die tijd de experimenten toch uit te voeren. Ik voelde me enigszins verbitterd en gedesillusioneerd over wetenschappelijk onderzoek. Want: wat nu? Terug naar het ziekenhuis? Opnieuw beginnen met een tweede postdoc? Waren er nog andere opties?
Mijn ziel verkopen!
Tijdens mijn opleiding Geneeskunde kregen we vrijwel alleen carrière paden aangeraden die naar het ziekenhuis leidden. Oftewel: je wordt dokter. Maar nu voelde ik een onverklaarbare weerstand tegenover een terugkeer naar het ziekenhuis om te werken als dokter. Omdat zowel wetenschap als patiënten mij drijven in mijn werk, overwoog ik een andere optie: de farmaceutische industrie.
De farmaceutische industrie staat binnen de opleiding Geneeskunde niet bepaald positief aangeschreven. Tijdens mijn werk als arts en onderzoeker ben ik grootgebracht met de quote: “Je verkoopt je ziel als je bij een farmaceut in dienst gaat”. Het belang van winst maken staat altijd boven het belang van de patiënt, werd altijd tegen ons gezegd.
Maar tijdens mijn postdoc merkte ik dat ook de wetenschap door pijnlijke punten geplaagd wordt. Het belang van je eigen CV/ een publicatie staat in veel gevallen ook boven de daadwerkelijke wetenschap. Als beiden waar zijn, wat was dan kwalijker? Of anders gezegd, als beide systemen ‘niet deugen’, welk systeem biedt dan de meeste mogelijkheden om wetenschap of patiënt verder te helpen? Aangezien ik volkomen onbekend was met de farmaceutische industrie en tot dusver enkel geleid werd door vooroordelen, besloot ik dus de stap de maken! Die naar de farmaceutische industrie.
Ziel verkopen?… niets is minder waar!
Een wereld ging voor me open, de wereld van klinisch onderzoek! Tijdens mijn eerste maanden heb ik vaak teruggedacht aan mijn eerdere ervaring bij het starten van mijn klinische opleiding in het ziekenhuis, de veelvoud aan afkortingen en protocollen vlogen me weer om de oren. Maar er was gelukkig ook veel ruimte, tijd en begeleiding om me wegwijs te maken in het landschap van de klinische studies. Er komt bizar veel kijken bij het ontwikkelen van nieuwe medicijnen. Van wetenschappelijke achtergrond, preklinische studies naar ontwikkeling en indiening van studieprotocollen bij FDA/ EMA, en van lokale wettelijke en ethische regulatie naar operationele aspecten en monitoren van effect en veiligheid… . En dit moet natuurlijk allemaal zo snel en efficiënt mogelijk, dus er is continue tijdsdruk. De drijfveer achter deze tijdsdruk is voelbaar en anders dan ik zo bevooroordeeld had ingeschat. De drijfveer is de patiënt!
Waarom duurt het dan toch vaak lang voor een nieuw medicijn beschikbaar is?
In onderstaande afbeelding is het klassieke standaardtraject te zien wat een potentieel nieuw geneesmiddel doorloopt. Het start in het succesvol doorlopen van preklinische studies waarbij je in kleinere proefdieren kijkt naar werkzaamheid en veiligheid maar ook in grotere proefdieren kijkt naar veiligheid. Pas nadat een potentieel geneesmiddel effectief (werkzaam tegen de aandoening die wordt behandeld) en veilig lijkt in preklinische studies, wordt het voor het eerst in mensen getest.
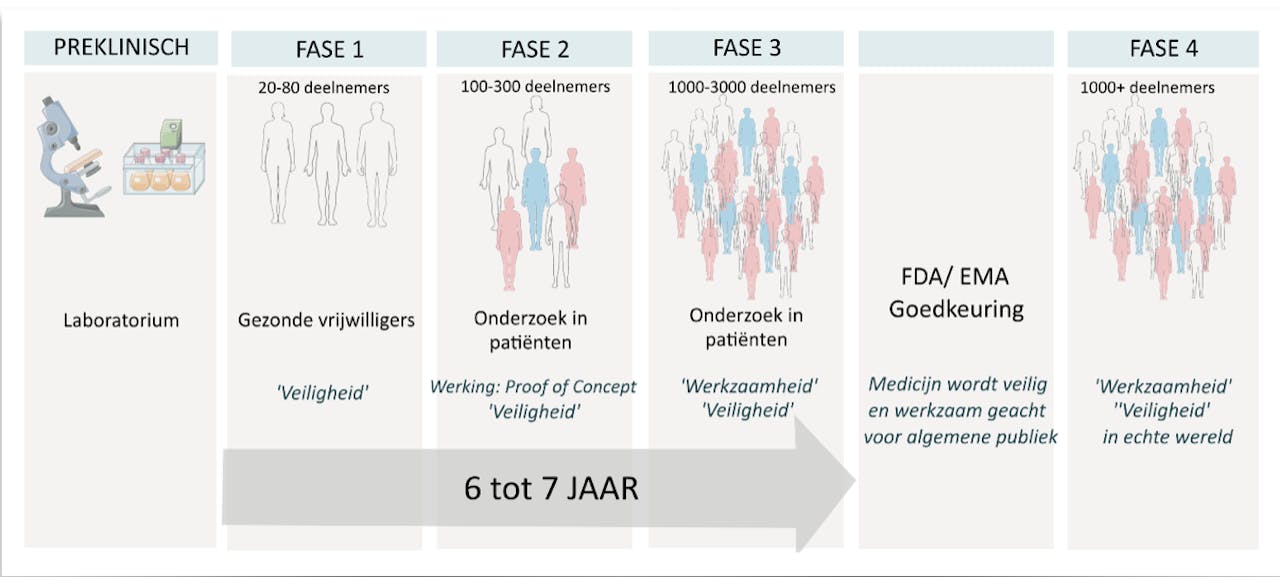
Klinische studie
Marieke Rienks voor NEMO KennislinkEen potentieel nieuw geneesmiddel heeft echter nog een lange weg te gaan voordat je het ook daadwerkelijk aan patiënten mag en kan geven. Dat het middel veilig en effectief in proefdieren blijkt, wil namelijk nog niet zeggen dat het medicijn ook veilig en effectief in mensen is. Om dit stapsgewijs te testen zijn er verschillende fasen van klinische studies. Zoals te zien in de afbeelding worden in elke volgende fase steeds meer mensen met het geneesmiddel getest.
Je kunt je wellicht voorstellen dat hoe meer mensen je blootstelt aan een nieuw geneesmiddel in een klinische studie om aan te tonen dat het middel effectief is, hoe groter de kans is dat je ook bijwerkingen gerelateerd aan veiligheid vindt. Het is dan erg belangrijk om te achterhalen of deze bijwerkingen te maken hebben met het geteste geneesmiddel. Pas als alle verschillende fasen van klinische studies zijn doorlopen, wordt een uitgebreid rapport ingediend bij de FDA/ EMA waarna het potentiele geneesmiddel al dan niet wordt goedgekeurd voor een bepaalde indicatie (ziekte).
Kan het korter?
Bij de ontwikkeling van nieuwe geneesmiddelen bestaat er een spanning tussen effectiviteit (werkzaamheid) en veiligheid van een nieuw geneesmiddel en de tijd die nodig is om alle door de FDA/EMA verplichte studies uit te voeren om dit te waarborgen. Met andere woorden: de tijd dat het middel beschikbaar is voor de patiënt. Ethische afwegingen spelen hierbij een belangrijke rol.
Neem als voorbeeld de aidscrisis van de jaren 90. De langdurige, veeleisende en bureaucratische goedkeuringsprocessen die destijds gepaard ging met het beoordelen van effectiviteit en veiligheid van nieuwe geneesmiddelen (wat ook weer mede het gevolg was van de geboorteafwijkingen bij kinderen van moeders die thalidomide ontvingen tijdens hun zwangerschap in de jaren 60), leek ethisch niet verantwoord voor patiënten met deze dodelijke ziekte.
Dit heeft onder andere geleid tot de versnellingen in het goedkeuringsproces voor nieuwe geneesmiddelen dat we nu kennen. Een vergelijkbare maatschappelijke en ethische afweging kunnen we nu maken bij de ontwikkeling van COVID-vaccins. De sterftecijfers en de economische gevolgen van de pandemie maken duidelijk hoe acuut de beschikbaarheid van vaccins is. Het doorlopen van alle verschillende studies ter waarborging van effectief en veiligheid van de vaccins lijkt daardoor wellicht onacceptabel lang. Versnelling van de procedures hoeft de veiligheid en effectiviteit niet in gevaar te brengen. Echter de voelbare druk op beschikbaarheid van vaccins maakt dat we allemaal indirect deelnemen aan het proces van de klinische studie. We zijn ons plots bewust van eventuele bijwerkingen gerelateerd aan veiligheid, nog voordat is vastgesteld of dit ook daadwerkelijk gerelateerd is aan het vaccin. Hier hebben we normaal geen weet van.
Samen staan we sterk!
Preklinisch onderzoek binnen de farmaceutische industrie is gericht op het vinden van nieuwe medicijnen. Preklinische onderzoek binnen academische instellingen is naast het vinden van nieuwe medicijnen wellicht meer gericht op het begrijpen van een gezond en ziek orgaan. Samenwerking lijkt mij van groot belang voor het doen van nieuwe ontdekkingen die potentieel tot betere behandelingen voor patiënten leiden. De academische instellingen missen immers vaak de geoliede en uitgebreide operationele infrastructuur om zo snel mogelijk een grote klinische studie van de grond te tillen. Het belangrijkst hierin blijft de patiënt.
Een samenwerking tussen patiënten, artsen en de farmaceutische industrie is dan ook essentieel om ervoor te zorgen dat de juiste wetenschappelijke innovaties zo snel EN veilig mogelijk bij patiënten terecht komen. Omdat ik beide werelden nu ken, weet ik inmiddels: om dit te bereiken is deelname aan klinische studies dus essentieel!

