In mijn onderzoek gebruik ik voornamelijk water als oplosmiddel. Water, H2O, is namelijk niet gevaarlijk voor ons of het milieu, en het is aanwezig in overvloed. Maar water is eigenlijk een heel speciaal goedje! In deze blog zet ik vijf gekke eigenschappen van water op een rijtje.
We drinken water, we zwemmen in water, en we spoelen de wc door met het kleurloze goedje. Water bedekt 70% van onze planeet, en wij hebben het allemaal nodig om in leven te blijven. Maar wat is het nu precies, en heeft het ook nog speciale eigenschappen? Eigenlijk is het een heel eenvoudige stof: het is niets meer dan een verbinding tussen een zuurstofatoom en twee waterstofatomen. Waterjuffers kunnen erover heen lopen en ijs blijft erop drijven. Hoe dit kan, heeft allemaal te maken met de bijzondere eigenschappen van water. Hieronder zet ik de vijf meest opvallende op een rijtje.
1. Water kent drie toestanden
Water is de enige stof die onder natuurlijke omstandigheden in drie toestanden voorkomt. Het kan voorkomen als ijs, zoals op de Noordpool, maar het kan ook een vloeistof zijn, zoals ons drinkwater, of een waterdamp, als je thee zet bijvoorbeeld. De temperatuurschaal van Celsius is zelfs gebaseerd op de overgang tussen deze toestanden: ijs smelt bij 0 °C en water kookt bij 100 °C.
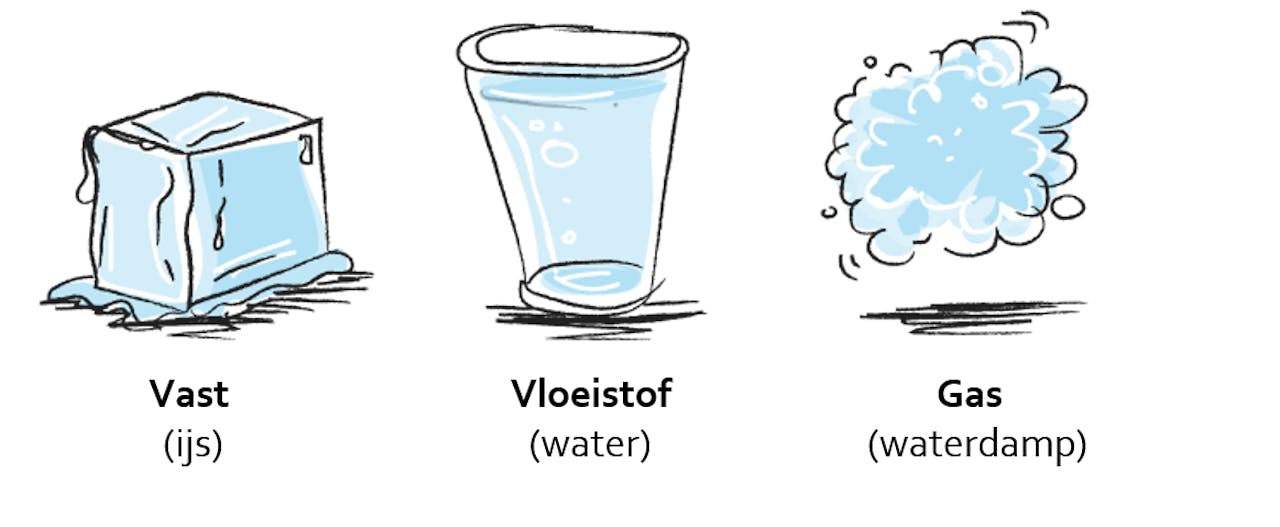
Water kent drie fasen: de vaste fase, vloeistoffase en gasfase.
natuur-en-techniek-oefenen.nl2. IJs drijft op water
Als je een handje steentjes in een beker water laat vallen, zul je zien dat alle steentjes zich naar de bodem verplaatsen. Dit is het geval met de meeste stoffen: de vaste stof is zwaarder en zinkt naar de bodem, terwijl de vloeistof erboven blijft drijven. In dat geval zou ijs ook moeten zinken. Maar niets is minder waar! De meest opvallende eigenschap van water is namelijk dat de dichtheid varieert met temperatuur.

IJs drijft op water.
MDV via Flickr CC BY-NC-ND 2.0Beneden 4°C zet het water uit, wordt het lichter en gaat het over in ijs. Omdat het ijs lichter is dan water, blijft het drijven in plaats van zinken. Dit is dus de reden waarom ijsblokjes bovenin je glas blijven drijven (en onhandig tegen je neus aanduwen tijdens het drinken), en waarom wij tijdens de koude wintermaanden lekker kunnen schaatsen terwijl visjes nog onder ons door kunnen zwemmen!
3. Eén voor allen en allen voor één.
Een andere belangrijke eigenschap van water is dat de moleculen graag bij elkaar blijven. Ze trekken elkaar aan via een speciale binding, de waterstofbrug. Dit is de verbinding tussen het zuurstofatoom van het ene watermolecuul en de waterstofatoom van het andere molecuul. Dankzij al die speciale bindingen ontstaat er een soort vlies, ook wel de oppervlaktespanning genoemd. Hierdoor blijven blaadjes drijven op het water, en kunnen kleine insecten, zoals de waterjuffer en poelschaatsenrijder, eroverheen lopen.

Wij kunnen schaatsen op ijs, maar kleine insecten schaatsen zelfs op water dankzij de oppervlaktespanning.
Arend from Netherlands, CC BY 2.0 via Wikimedia CommonsJe kunt deze eigenschap ook gemakkelijk zelf testen door een paperclip voorzichtig in een glas water te laten zakken: dankzij de oppervlaktespanning blijft hij drijven.
4. Water is zowel een zuur als een base
Zuiver kraanwater is pH neutraal (pH = 7), en is daardoor niet zuur, zoals citroensap, maar ook niet basisch, zoals zeep. En toch kan het zich als zuur (pH < 7) én als base (pH > 7) gedragen! Een gulle watermolecuul is namelijk in staat om één van zijn waterstofatomen te doneren aan een ander molecuul, waardoor het handelt als een zuur. Aan de andere kant kan een grijpgrage watermolecuul een waterstofatoom van een ander molecuul afpakken, waardoor het zich gedraagt als een base. Dus, afhankelijk van de omstandigheden, gedraagt water zich als een grijpgrage base of als een vrijgevig zuur.
5. Water is een universeel oplosmiddel
Water staat bekend als het ‘universele oplosmiddel’ bij uitstek, niet omdat het alles oplost, maar wel omdat het veel meer stoffen kan oplossen dan enig ander oplosmiddel. Dit is een zeer belangrijke eigenschap voor alle levende wezens op onze aarde. Water is namelijk overal om ons heen, en het is in staat om essentiële stofjes (mineralen, zouten, voedingsstoffen) op te lossen en met zich mee te nemen, ongeacht of het zich voortbeweegt in de lucht, over de grond of in onze lichamen.
/a>
Water als universeel oplosmiddel.
Deze eigenschap komt door de chemische structuur. Watermoleculen zijn namelijk polair: water is aan één kant deels positief geladen (het waterstofatoom) en aan de andere kant deels negatief (het zuurstofatoom), waardoor het veel verschillende moleculen kan aantrekken en oplossen.
BONUS: Een extra zuurstofatoom maakt water giftig
Als je een extra zuurstofatoom aan een watermolecuul toevoegt, krijg je waterstofperoxide (H2O2). In tegenstelling tot water, is waterstofperoxide giftig, zeer reactief en zeker niet drinkbaar. Het wordt voornamelijk gebruikt als bleekmiddel, oxidant of ontsmettingsmiddel. Zo maakt waterstofperoxide ons haar blonder (zoals dat van Marilyn Monroe), of zorgt het voor een schoon en wit gebit.
Dankzij al deze eigenaardige, maar tegelijkertijd ook cruciale eigenschappen, is het watermolecuul mijn lievelingsmolecuul geworden.

