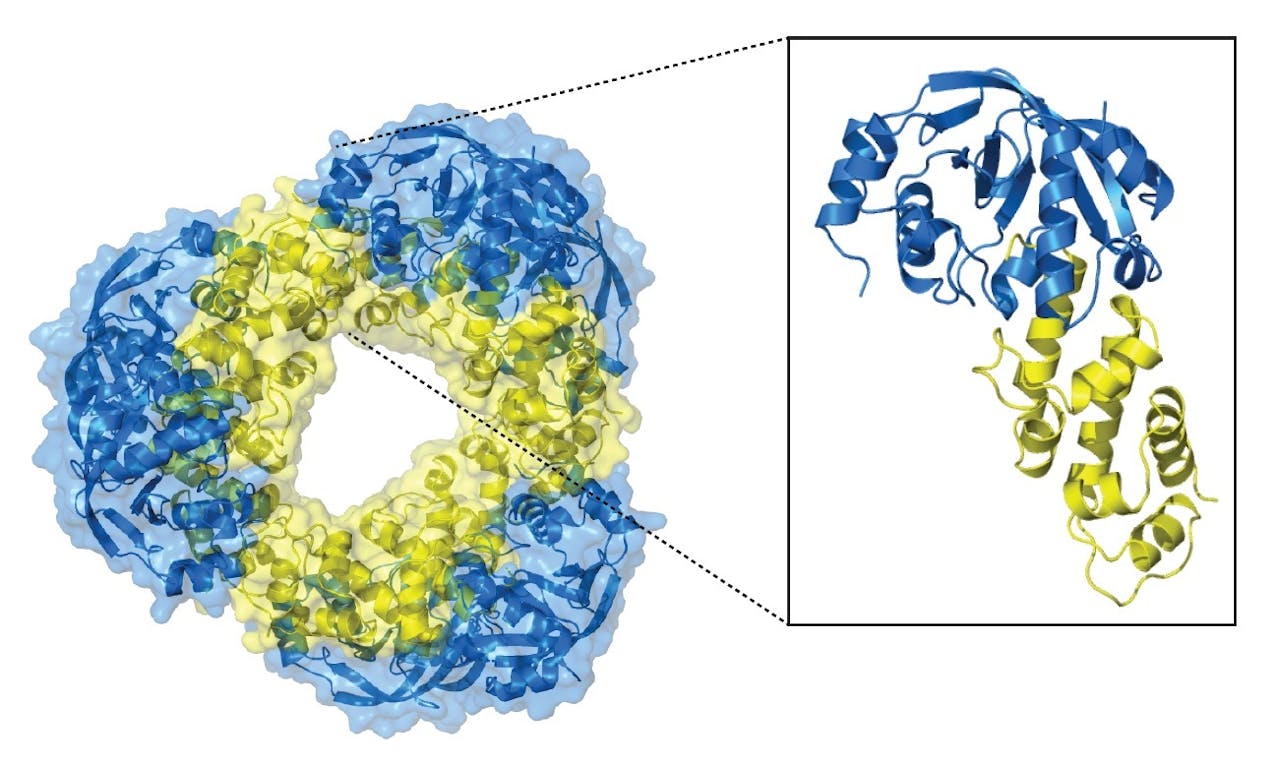
Een team van Europese wetenschappers heeft een gif-antigif-systeem van de tuberculosebacterie gedetailleerd in beeld gebracht. Verstoring van dit systeem zorgt ervoor dat de bacterie doodgaat. Dat biedt aanknopingspunten voor de zoektocht naar nieuwe medicijnen tegen tuberculose.
Tuberculose is wereldwijd nog steeds een groot probleem. In 2017 werden er tien miljoen mensen ziek door een infectie met Mycobacterium tuberculosis. Daarvan stierven er bijna anderhalf miljoen. De tuberculosebacterie veroorzaakt ontstekingen, vooral in de longen maar soms ook in andere delen van het lichaam. De belangrijkste symptomen zijn langdurig hoesten, vermoeidheid en koorts.
Bijzonder systeem
“Mycobacterium tuberculosis is lastig te bestrijden”, vertelt Annabel Parret, onderzoeker aan het European Molecular Biology Laboratory in Hamburg. “De bacterie heeft een heel stevige celwand. Hij bouwt als het ware een enorme muur om zichzelf heen. Antibiotica komen daar heel moeilijk doorheen.” De bacterie beschikt, net als sommige andere bacteriën, wel over verschillende gif-antigif-systemen. Dit zijn verzamelingen van genen die coderen voor zowel een giftig eiwit als een eiwit dat de gifstof kan afbreken.
Onder normale omstandigheden blokkeert het antigif de werking van het giftige eiwit en kan de bacterie goed groeien. In tijden van stress, bijvoorbeeld als er weinig voedingsstoffen beschikbaar zijn, breken speciale enzymen het antigif af. Daardoor krijgt het giftige eiwit de vrije hand en wordt de groei van de bacterie geremd. Mycobacterium tuberculosis heeft één heel bijzonder gif-antigif-systeem (zie kader). Het gif dat uit dit systeem vrijkomt, zorgt ervoor dat de bacterie doodgaat.
Heel wat eisen
Parret en haar team hebben dit zelfmoordsysteem nu gedetailleerd in beeld gebracht. Door te kijken naar de 3D-structuur van de verschillende eiwitten en deze te vergelijken met andere structuren, ontdekten de wetenschappers dat het gif NAD+ onschadelijk maakt. “NAD+ is een essentieel molecuul in alle levende organismen”, legt Parret uit. “In bacteriën, maar ook in bijvoorbeeld dierlijke cellen, worden veel reacties geregeld door NAD+-achtige stoffen. Dit is een algemeen principe. Als we het gifeiwit van de tuberculosebacterie inspuiten in zebraviseitjes gaan die ook dood.”
De uitdaging is nu om dit bijzondere zelfmoordsysteem in te zetten om tuberculose te bestrijden. De wetenschappers gaan de komende jaren op zoek naar stofjes die de werking van het gif-antigif-systeem kunnen blokkeren. Dat klinkt eenvoudiger dan het is, want zo’n stofje moet aan heel wat eisen voldoen. Ten eerste moet het stofje in staat zijn om de bacterie binnen te dringen. Daarnaast moet het stofje stabiel zijn. Het moet niet direct uit elkaar vallen en het moet het gifeiwit voor langere tijd actief houden zonder dat de bacterie zich daartegen kan beschermen.
Als laatste moet het stofje geen bijwerkingen geven. Activeren van een gif dat het essentiële molecuul NAD+ onschadelijk maakt, is niet zonder risico’s. Parret weet zeker dat het gifeiwit niet spontaan uit de tuberculosebacterie ontsnapt, maar weet nog niet zeker wat er met het gif gebeurt als de bacterie doodgaat. Kan het gif zich dan vrij door het lichaam bewegen? “We zien dat niet gebeuren als tuberculosebacteriën sterven in een kweek van menselijke afweercellen”, stelt ze. “Ik denk dus dat het eiwit zijn activiteit verliest zodra de bacterie dood is.” Als die aanname klopt, vergroot dat de kans op de ontwikkeling van een nieuw medicijn tegen tuberculose.