Vanuit stamcellen kraakbeencellen maken is al een tijdje mogelijk. Maar er was altijd een probleem. De gemaakte kraakbeencellen groeien na een tijdje allemaal uit tot bot. Wetenschappers van de Universiteit Twente zijn er nu voor het eerst in geslaagd om kraakbeencellen te kweken die daadwerkelijk kraakbeen blijven. Een lage zuurstofconcentratie bleek de sleutel tot succes.
“De omzetting van kraakbeen naar bot is een heel natuurlijk proces”, vertelt Marcel Karperien, bioloog aan het Twentse MIRA-instituut. “Als je kijkt naar de embryogenese, het ontwikkelingsproces van een embryo in de baarmoeder, zie je dat nagenoeg ons hele skelet eerst in kraakbeen wordt aangelegd. Daarna volgt de omzetting naar bot. Er is één uitzondering. Helemaal aan het uiteinde van het bot zitten stukjes kraakbeen die kraakbeen blijven. Die stukjes fungeren als stootkussentjes voor de gewrichten en zorgen ervoor dat we soepel kunnen bewegen. Bij osteoartrose is dat kraakbeen verdwenen en gaat het bot op bot bewegen. Dat veroorzaakt pijn.”
Bloedvaatjes
Het kweken en implanteren van nieuwe stootkussentjes zou een manier kunnen zijn om artrose te behandelen. Maar dat is nog niet zo makkelijk. Karperien: “Wat wij, en collega’s uit andere laboratoria, al heel lang kunnen is het opkweken van beenmergstamcellen (mesenchymale stamcellen). Daar kunnen we vervolgens vet, bot en kraakbeen van maken. Maar het kraakbeen dat je op die manier maakt, heeft alle kenmerken van kraakbeen dat later verandert in bot. Dat zagen we dus ook steeds gebeuren. Wat we nog niet konden, was die andere vorm van kraakbeen maken; kraakbeen dat kraakbeen blijft.”
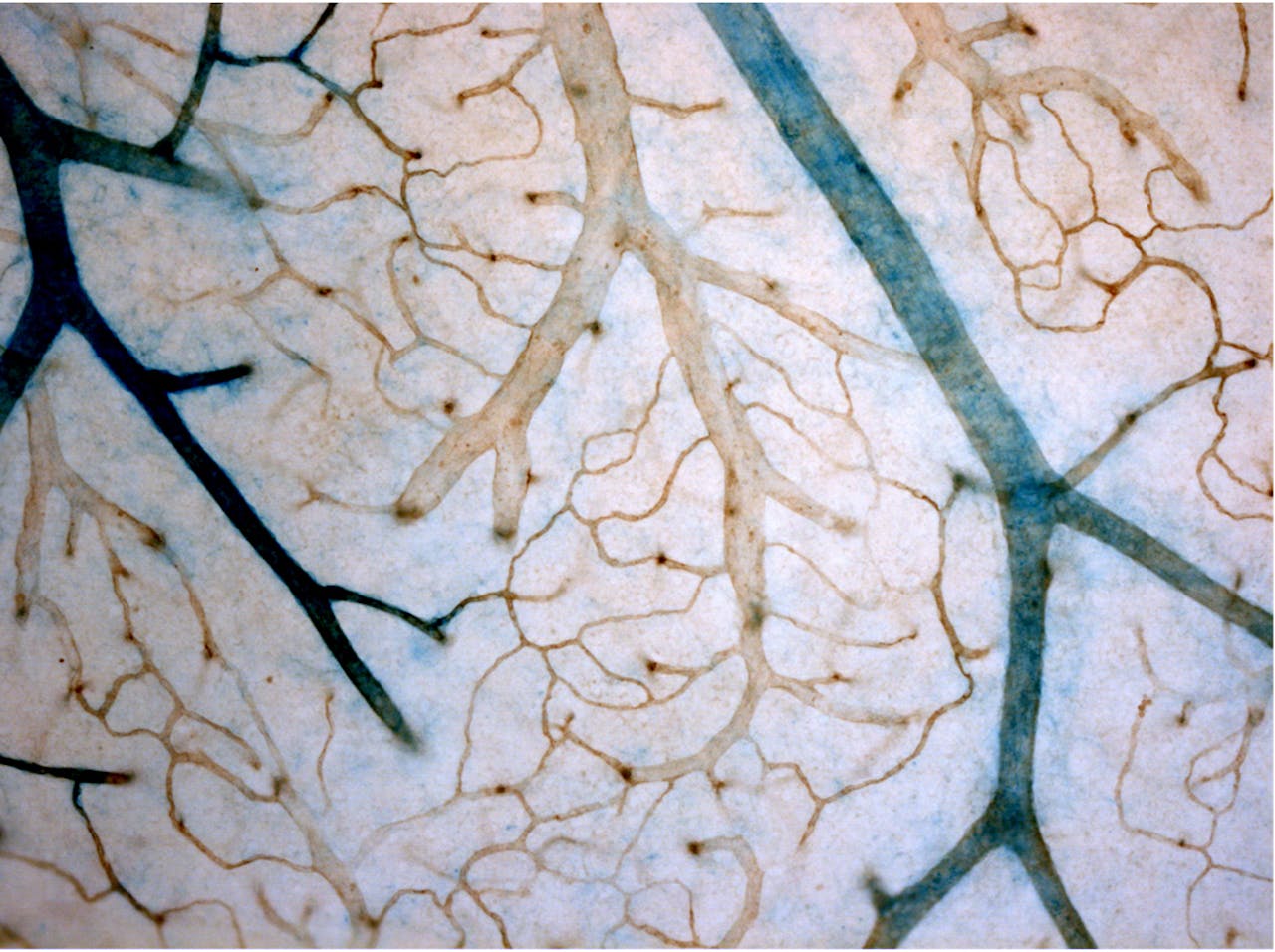
Hoe meer bloedvaatjes, hoe meer bot. In het kraakbeen dat kraakbeen blijft, vind je dan ook nauwelijks bloedvaatjes.
Science/AAASEn dat is de Twentse onderzoekers nu wel gelukt, door heel goed te kijken naar de kraakbeenontwikkeling in embryo’s. Er bleek een associatie te zijn tussen het aantal bloedvaatjes dat het kraakbeen ingroeit en de hoeveelheid botvorming. Hoe meer bloedvaatjes, hoe meer bot. “Bloedvaatjes zijn de zuurstofleveranciers van ons lichaam, dus misschien is een lage zuurstofconcentratie voor kraakbeencellen wel de trigger om kraakbeen te blijven”, legt Karperien uit. “Deze hypothese zijn we gaan testen.”
2,5 procent zuurstof
Met relatief simpele apparatuur kweekten de wetenschappers stamcellen onder een zuurstofconcentratie van 2,5 procent. Dat is aanzienlijk lager dan de concentratie van 21 procent, waar cellen normaal gesproken onder gekweekt worden. Die 21 procent is de hoeveelheid zuurstof in de atmosfeer, maar dat is volgens Karperien al een vreemde omgeving om in te gaan kweken. “In het lichaam is de zuurstofconcentratie al veel lager. En in het gewrichtskraakbeen is het vaak nog lager dan in de rest van het lichaam. Vandaar die 2,5 procent.”
De onderzoekers implanteerden hun gemaakte cellen bij muizen en volgden de ontwikkeling van het kraakbeen vijf weken lang. Kraakbeen dat gekweekt werd onder een zuurstofconcentratie van 2,5 procent bleef kraakbeen, terwijl kraakbeen dat gekweekt werd onder een zuurstofconcentratie van 21 procent veranderde in bot.
Karperien: “Zuurstof is dus een sturende factor in het lot van kraakbeencellen.” En dat heeft gevolgen voor andere laboratoria die met kraakbeencellen werken of zich ook bezighouden met de regeneratie van kraakbeen. “Leveranciers van de apparatuur die we gebruikt hebben, zullen wel blij zijn met onze publicatie”, grapt hij. “Want ook al werkt kweken onder een lage zuurstofconcentratie iets lastiger, ik denk dat veel labs deze apparatuur nu wel zullen gaan kopen, als ze dat al niet gedaan hebben.”
Lang traject
Volgens de bioloog brengt deze ontdekking de behandeling van kraakbeenziekten, zoals artrose, een stap dichterbij. “Het is een grote stap voorwaarts, maar er zijn ook nog veel stappen nodig om uiteindelijk een product te kunnen maken waar patiënten wat aan hebben”, zegt hij. “Wij hebben de kraakbeencellen nu geïmplanteerd bij muizen en dat vijf weken lang gevolgd, maar bij een mens moet het kraakbeen natuurlijk een leven lang meegaan. We moeten het kraakbeen nu gaan implanteren in het gewricht van een groter proefdier, zoals een geit of schaap. Pas als daar het beoogde resultaat wordt bereikt en er zijn geen nare bijeffecten, kunnen we gaan denken over een toepassing bij de mens. Dat is nog een lang traject.”
Karperien denkt dat het spelen met de zuurstofconcentratie in het algemeen een goede methode is om de differentiatie van stamcellen te beïnvloeden. “We weten dat niet elk weefsel even goed doorbloed is. Wij hebben nu specifiek gekeken naar kraakbeen, maar wellicht is de ontwikkeling van andere type weefsels vanuit stamcellen ook te optimaliseren door de zuurstofconcentratie te verlagen.”

