Een moleculaire motor kun je prima inzetten als een boormachine. De draaiende ‘kop’ boort zich soepel door de celmembraan, waardoor levende cellen snel het loodje leggen, zo laat een publicatie in Nature zien. Volgens de onderzoekers biedt dit zicht op een geheel nieuwe vorm van chemotherapie.
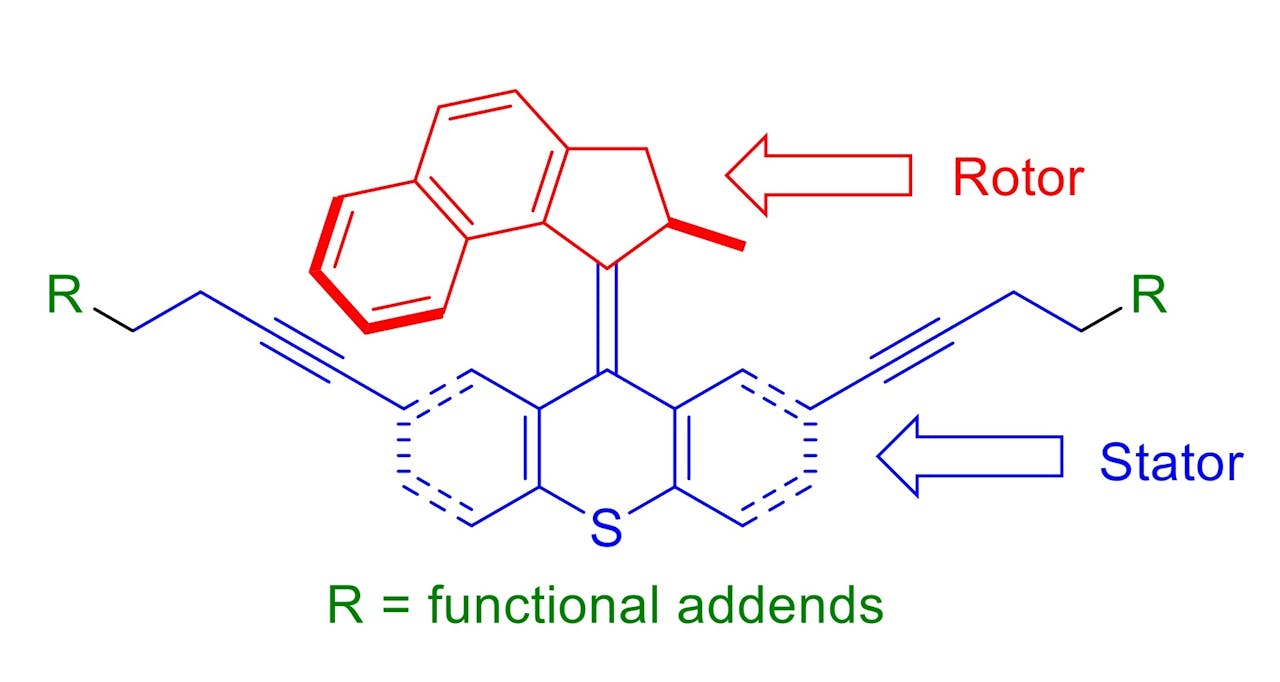
Een dodelijke boormachine wekt misschien associaties op met een slechte horrorfilm, maar de moleculaire boormachine die James Tour, hoogleraar aan Rice University in Texas en collega’s in het tijdschrift Nature presenteren, is dodelijk op een goede manier. Ze gebruiken een moleculaire motor zoals die is ontwikkeld door de Groningse hoogleraar en Nobelprijswinnaar Ben Feringa. De motor van Tour en zijn team zorgt echter niet voor de aandrijving van een nanoauto of ander vehikel, maar werkt als een supersnelle moleculaire boormachine die door z’n draaiing gaten kan boren in de celmembraan, de ‘wand’ van de cel.
Gaten boren blijkt in hun experimenten een effectieve manier om levende cellen het loodje te laten leggen. Het duurt ongeveer een minuut voordat de moleculaire boormachine zichzelf dwars door de celmembraan heeft gewerkt. De boor draait met zeer hoge snelheid, ongeveer twee tot drie miljoen maal per seconde, en duwt de moleculen waar de membraan uit bestaat simpelweg aan de kant.
Weglekken
De celmembraan is een beweeglijk, vettig laagje waar continu allerlei moleculen (voedingstoffen, afval) doorheen gaan. Het is geen ondoordringbare barrière, maar het transport via poriën in de membraan is wel strikt gecontroleerd. De boor gaat echter zo heftig tekeer, dat de membraan de controle verliest. “De schade die boor aanricht is enorm en de celmembraan sluit zich niet snel genoeg om het weglekken van de inhoud van de cel te voorkomen”, laat James Tour desgevraagd weten. “De noodzakelijke verschillen tussen de binnenkant en buitenkant van de cel, die de celmembraan normaal gesproken in stand houdt, raken dusdanig verstoord dat herstel onmogelijk wordt.”
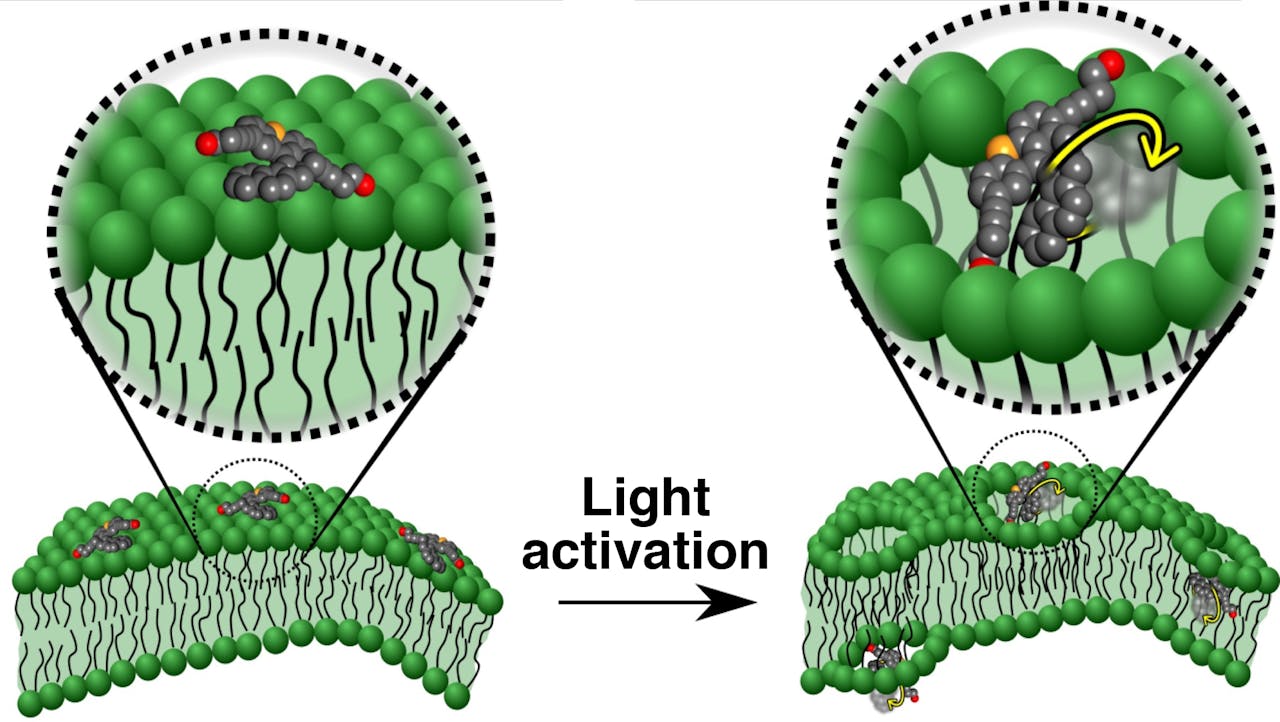
Schematische weergave van de moleculaire boormachine. Eenmaal gehecht aan de celmembraan en dan geactiveerd, boort het draaiende deel van het molecuul (grijs) zich een weg door de celmembraan (groene bolletjes met zwarte staarten). De gaten gaan niet snel genoeg dicht om het leeglopen van de cel te stoppen. De cel sterft.
Tour Group/Rice UniversityDubbele veiligheid
Tour ziet allerlei medische toepassingen voor de moleculaire boormachine, met name om kankercellen te lijf te gaan. In het Nature-artikel beschrijven de auteurs de succesvolle werking van de boor tegen onder meer levende, menselijke prostaatcellen. Een bekend probleem bij het ontwikkelen van nieuwe therapieën tegen kanker is dat het moeilijk is om onderscheid te maken tussen gezonde cellen en kankercellen. Met als gevolg dat ook veel gezond weefsel ernstig wordt aangetast. Tour en zijn team proberen dat met een dubbel veiligheidssysteem te ondervangen. Ze laten zien dat je aan het niet draaiende deel van de boormachine ‘staarten’ kunt vastmaken die heel specifiek aan bepaalde cellen binden. Dat is op zich geen nieuwe aanpak, ook veel huidige chemokuren worden al gekoppeld aan bijvoorbeeld antilichamen die ervoor (moeten) zorgen dat alleen kankercellen de volle laag krijgen.
De extra veiligheid bij de boormachine zit in de ‘aan/uit-knop’. Moleculaire motoren draaien niet uit zichzelf, ze hebben een energiebron nodig – net zoals een auto brandstof nodig heeft en een boormachine stroom. Bij moleculaire motoren is licht de meest gebruikte energiebron. Alleen als er licht van de juiste golflengte op het molecuul valt, gaat de motor draaien. “Dat geeft extra controle”, aldus Tour. “De lichtbundel kun je heel specifiek richten op de plaats waar de boormachines in actie moeten komen. Eventuele boormachines die op andere, ongewenste plaatsen toch zijn gaan plakken, bevinden zich niet daar waar de lichtbundel schijnt en zullen dus niet gaan draaien.”
Nieuw type chemo
Spectaculaire resultaten in een schaaltje met wat cellen zijn geen enkele garantie voor een succesvol geneesmiddel. Aan de boormachines moet nog heel wat gesleuteld worden, bijvoorbeeld op het gebied van de activatie door licht. Daarvoor gebruiken ze nu nog uv-licht, maar daar kleven allerlei nadelen aan. Het is schadelijk voor levende cellen en bovendien kan het niet diep doordringen in weefsels. Er moet dus in ieder geval een andere aan/uit-knop komen. Ook het richten van de boormachine op de gewenste cellen is in een levend organisme met allerlei verschillende soorten cellen een lastige klus. Desalniettemin is Tour hoopvol gestemd. “Ik zie dit echt als een compleet nieuw type chemotherapie. Het is een geheel nieuw mechanisme, dat ook voor andere ziekten relevant is. Niet alleen om cellen direct te doden, maar bijvoorbeeld om geneesmiddelen in de cel te krijgen via de openingen die de boormachine maakt.”