Soms kun je met oude bekenden compleet nieuwe ontdekkingen doen. In het tijdschrift Science laten chemici van de Rijksuniversiteit Groningen zien hoe met twee honderd jaar oude methoden de synthese van een belangrijke groep stoffen voor geneesmiddelen veel eenvoudiger en preciezer wordt.
Hoeveel verschillende moleculen ze ook hebben gemaakt, voor chemici als Syuzanna Harutyunyan lonkt er altijd wel weer een nieuw molecuul aan de horizon. In dit geval trokken de gefunctionaliseerde heterocyclische aromaten haar aandacht. Dit zijn moleculen met een ringvormige (aromatische) structuur die ook andere atomen dan koolstof bevat (heterocyclisch) en met bovendien nog extra groepen aan de ring gekoppeld (gefunctionaliseerd).
Het overgrote deel, bijna negentig procent, van alle nu bekende actieve farmaceutische ingrediënten bevat zo’n gefunctionaliseerd heterocyclisch aromatisch element. Er is daarom veel interesse om nog meer variaties op dit type molecuul te kunnen maken. Wie weet zit er een nieuw medicijn tussen.
Grignard reagens
Maar het probleem zit in het koppelen van de functionele groep die voor de variatie zorgt. “Als startpunt worden moleculen met de ringvormige elementen gebruikt. Die zijn makkelijk te maken, maar helaas zijn ze nauwelijks reactief. Alleen onder extreme condities lukt het om een functionele groep eraan te koppelen”, vertelt Harutyunyan, adjunct hoogleraar aan het Stratingh Instituut voor Chemie, Rijksuniversiteit Groningen. “Het bijzondere van onze benadering is dat het is gelukt om in één stap vanuit deze niet-reactieve stoffen het gewenste eindproduct te vormen onder vrij gangbare omstandigheden.”
De oplossing voor het probleem vroeg wel meerdere stappen. De eerste stap was het gebruik van een zogeheten Grignard reagens. Daar is overigens niets nieuws aan; de Franse chemicus François Grignard kreeg al in 1912 de Nobelprijs voor de ontdekking van de naar hem genoemde stoffen. “Ik werk al lange tijd met Grignard reagentia. Die zijn heel reactief en worden veel gebruikt om koolstof-koolstofbindingen te maken.” De reactie tussen het Grignard reagens en de uitgangsstof verliep bij kamertemperatuur echter volstrekt anders dan verwacht. Er gebeurde helemaal niets.

Temperatuur omlaag
Harutyunyan deed nog een keer een greep in de chemische historie en koos voor een Lewiszuur om de reactiviteit te bevorderen. Volgens de theorie van de Amerikaanse chemicus Gilbert Lewis, een tijdgenoot van Grignard, kan ieder molecuul dat elektronen aantrekt beschouwd worden als een zuur. Ook de Lewiszuren en -basen zijn bekende namen in de organische synthese. “Het gebruik van een Lewiszuur is zeker niet nieuw, maar in deze context was het wel een vernieuwende keuze.”
Een keuze die volgens veel collega-scheikundigen niet kon werken. Grignard reagentia zijn basisch en zullen dus meteen reageren met een sterk Lewiszuur. En niet met de uitgangsstof zoals het plan was. “Uit eerder werk wist ik dat het wel kon, maar alleen bij een zeer lage temperatuur. De reactiviteit van zowel het Grignard reagens als het Lewiszuur neemt dan sterk af en dat is precies wat je hier nodig hebt. Want dan blijft er genoeg tijd over om de gewenste reactie te laten plaatsvinden.” Daarmee was ze er nog niet, want de functionele groep moet steeds op dezelfde ‘kant’ van het koolstofatoom worden gezet.
Spiegelbeeld
Als er aan een koolstofatoom vier verschillende groepen zijn gebonden heet dit een asymmetrisch of chiraal centrum. Je krijgt dan twee ruimtelijke oriëntaties die sprekend op elkaar lijken, maar elkaars spiegelbeeld zijn. Net zoals je linker- en rechterhand. Dat maakt heel vaak niet uit, maar juist voor toepassing in geneesmiddelen is het extreem belangrijk. Voor de biologische werking kan het een groot verschil maken of je met de linkerhand of de rechterhand te maken hebt. Daarom is het voor de synthese van farmaceutische stoffen cruciaal dat er slechts één van de twee vormen wordt gemaakt.
Harutyunyan had dus nog een asymmetrische katalysator nodig; een hulpstof die ervoor zorgt dat de functionele groep slechts op één manier wordt aangekoppeld. Ook hiervoor kon ze putten uit een breed aanbod en een koperhoudende katalysator gaf de beste resultaten. “Het was nog wel spannend of de katalysator geen last zou hebben van het Lewiszuur, maar dat pakte goed uit.”
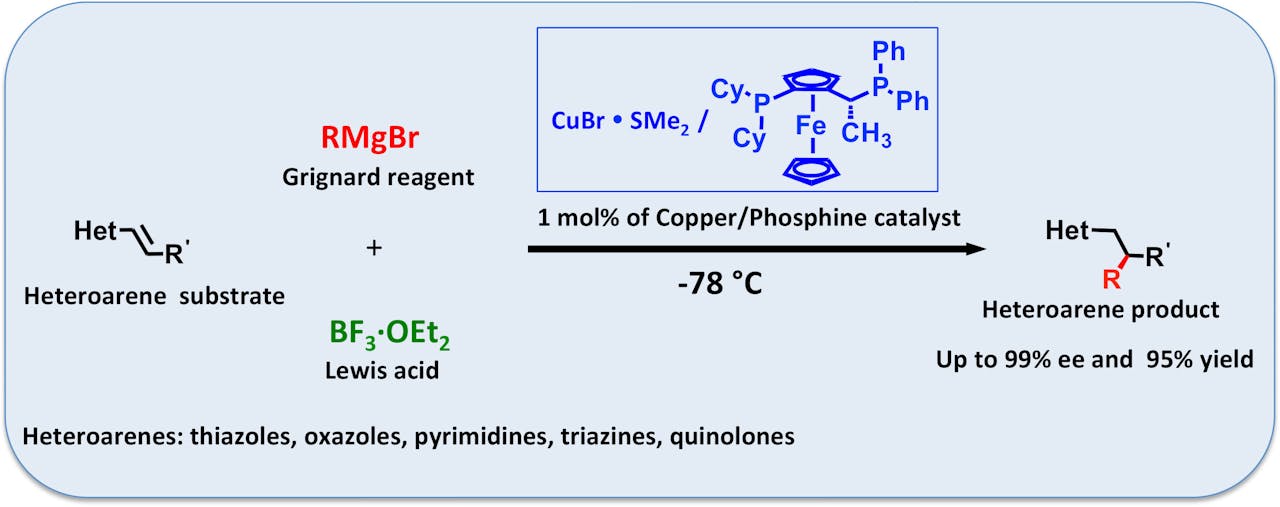
Links de uitgangsstof, waarbij ‘Het’ staat voor een grote collectie aan ringvormige structuren die naast koolstof ook andere atomen bevatten, zoals stikstof, zuurstof of zwavel. Met R’ wordt iedere willekeurige zijketen bedoeld. Het rode RMgBr is het Grignard reagens. R is hier de functionele groep waar het allemaal om draait; die wil je koppelen aan de uitgangsstof. Mg is magnesium, Br is broom. Het groene BF3OEt2 is het Lewiszuur. B is boor, F is fluor, O is zuurstof. Et betekent ethyl, een zijketen van twee koolstof en vijf waterstofatomen (-CH2CH3). In het blauw staat de katalysator afgebeeld, een complexe structuur met onder meer koper (Cu) en ijzer (Fe). Al deze stoffen samen bij een temperatuur van minus 78 graden geeft het eindproduct Het-R-R’.
S. Harutyunyan/RuG (met toestemming)Met deze combinatie van Grignard reagens, Lewiszuur, asymmetrische katalysator en een lage temperatuur van -78°C lukte het Harutyunyan en haar team om aan een hele reeks van uitgangsstoffen een functionele groep toe te voegen. Met in vrijwel alle gevallen een hoge voorkeur voor slechts één spiegelbeeldvorm. De opbrengst vertoonde nogal wat variatie, afhankelijk van de gekozen uitgangsstof.
“Dat komt doordat er in sommige gevallen nevenreacties optreden. De functionele groep wordt wel op de juiste plek gekoppeld, maar ook op andere plekken in de uitgangsstof. Daar kwamen we achter toen we goed in het mechanisme van de reactie doken, maar toen hadden we deze publicatie al geschreven.” Die ontdekking is overigens de moeite waard. “We werken daar nu verder aan, omdat we denken hier weer nieuwe chemische mogelijkheden uit te halen. Dat we bijvoorbeeld meerdere asymmetrische centra kunnen inbouwen in een molecuul. Dat is heel interessant.”
Bibliotheken
De belangrijkste toepassing voor deze nieuwe synthese methode ligt in de farmaceutische industrie. Daar maken ze grote ‘bibliotheken’ van verschillende moleculen om die vervolgens te testen op een bepaalde activiteit en zo nieuwe interessante stoffen voor geneesmiddelen te ontdekken. Is de methode van Harutyunyan ook toepasbaar voor dit doel?
“Dat is een goed punt, het was ook een van de commentaren die we kregen op ons artikel. We hebben daarom wat zaken aangepast. Zoals het oplosmiddel. Eerst werkten we met ether, maar dat is verboden in de industrie vanwege de brandbaarheid. Inmiddels weten we dat andere gangbare oplosmiddelen net zo goed werken, dus dat probleem is aangepakt.” En ook de lage temperatuur kan wel iets minder laag zijn, weten ze nu. “We zijn er ondertussen in geslaagd de temperatuur naar min vijftig te brengen, zonder verlies aan selectiviteit en opbrengst. De industrie wil graag naar min veertig, maar daar zijn we nog niet.”
Ze heeft wel een idee voor een oplossing. “Een van de problemen die je krijgt bij hogere temperaturen is dat de reactiviteit van je uitgangsstof weer afneemt doordat het Grignard reagens en het Lewiszuur juist veel reactiever worden en vooral met elkaar gaan reageren. Maar ik denk dat we het Lewiszuur in veel kleinere hoeveelheden kunnen gebruiken, net als je bij een katalysator doet. Het zou me niet verbazen als dat werkt. Hoe dan ook denk ik dat dit probleem oplosbaar is. We hebben deze methode nog maar net ontdekt en staan nog helemaal aan het begin van de verdere ontwikkeling en verfijning.”

