‘Batterijveteraan’ John Goodenough komt op 94-jarige leeftijd met een mogelijk nieuwe batterijrevolutie: een accu zonder vloeibare onderdelen met een capaciteit die vele malen hoger ligt dan de huidige batterijen. Andere onderzoekers zijn sceptisch.
Ze vervullen een essentiële rol in de wereld: lithium-ion-batterijen. Door hun betrouwbaarheid en hoge energiedichtheid vind je ze terug in vrijwel alles wat oplaadbaar is. Van mobiele telefoons en laptops tot elektrische auto’s. Geheel zonder nadelen zijn ze overigens niet: bij een te snelle laadsessie kan er kortsluiting ontstaan, waarbij de batterij sterk opwarmt en openbarst. Dit probleem teisterde de uit de schappen gehaalde Samsung-telefoon Galaxy Note 7.
Een groep van wetenschappers van onder andere de Universiteit van Texas zegt nu een alternatief te hebben. Onder leiding van onderzoeksveteraan John B. Goodenough – die betrokken was bij de ontwikkeling van de lithium-ion-batterij – claimen ze een nieuwe lithiumbatterij te hebben die enkel uit vaste onderdelen bestaat. Het doorgaans vloeibare elektrolyt is vervangen door een glasachtig materiaal, waardoor kortsluiting vrijwel is uitgesloten. Als klap op de vuurpijl slaat de batterij bijna viermaal zoveel energie op als haar huidige concurrenten. Het onderzoek werd gepubliceerd in het gerespecteerde tijdschrift Energy & Environmental Science. Hierna barstte er een golf van kritiek los.
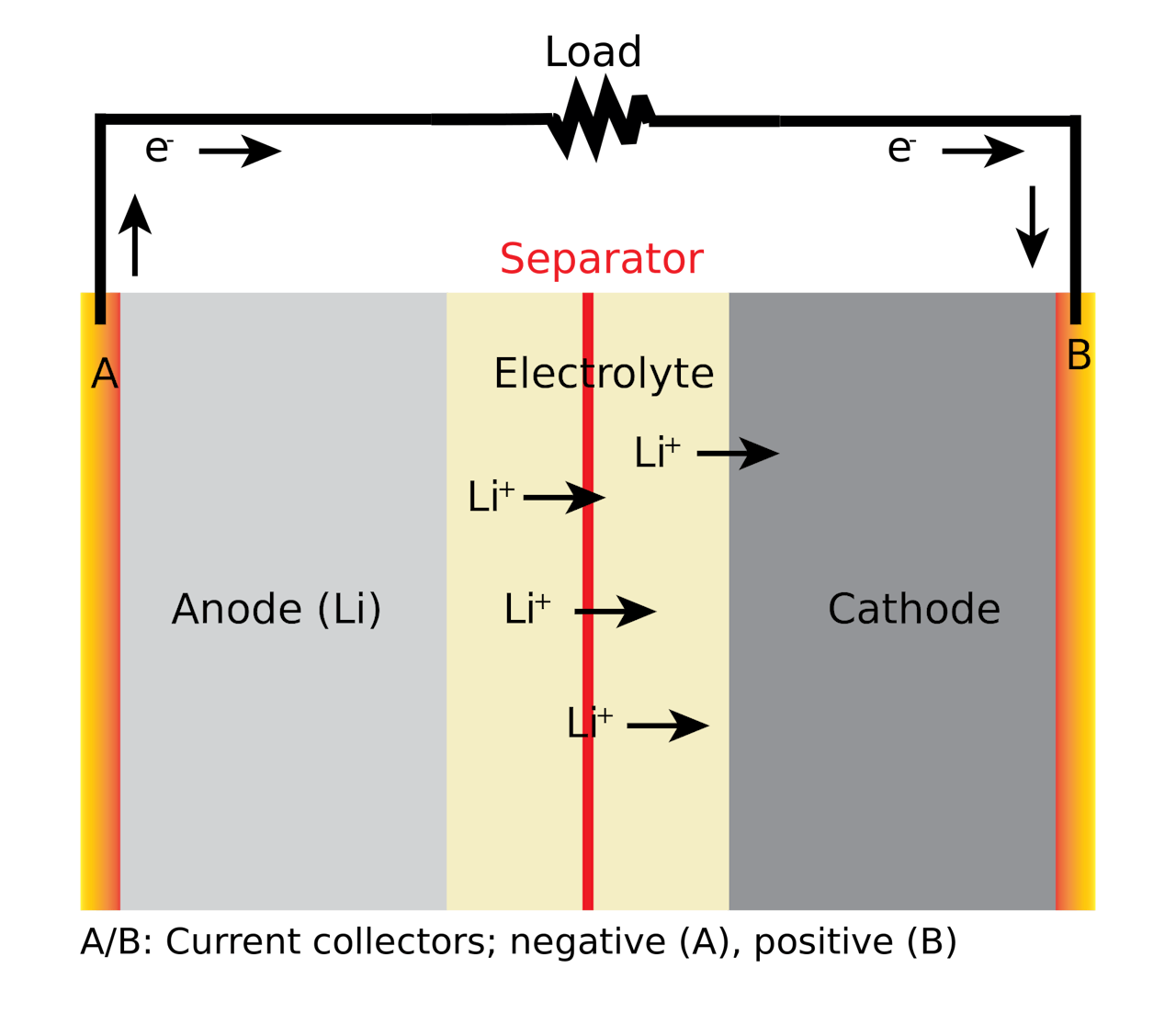
De werking van een lithium-batterij, vergroot voor uitleg.
Sdk16420 via CC BY-SA 4.0Ionen en elektronen
Om Goodenoughs vinding te snappen, ontkomen we niet aan een kleine batterijles. Een batterij bestaat altijd uit twee compartimenten (de zogenoemde anode en kathode) die worden gescheiden door een barrière (het elektrolyt). Een lithium-ion-batterij wordt gedreven door chemische reacties waarbij positief geladen lithiumdeeltjes (lithiumionen) van het ene naar het andere compartiment reizen. Tegelijkertijd reizen er negatief geladen elektronen in dezelfde richting, maar zij moeten door een draad heen. Het is deze elektronenstroom die een apparaat aandrijft.
De batterijprestatie hangt af van de gebruikte materialen. Hoe meer lithiumionen het systeem kan opslaan en verplaatsten, des te groter is de capaciteit van de batterij. Bij een oplaadbare batterij moeten de chemische reacties bovendien volledig omkeerbaar zijn. Het liefst zou je als anode een blokje puur lithium gebruiken (daarin zit immers het meeste lithium), maar dat levert problemen bij het opladen. Het lithium groeit dan als lange vertakkingen terug op de anode. Gevaarlijk, want wanneer de twee elektrodes via zo’n ‘lithiumtak’ met elkaar verbonden worden, ontstaat er kortsluiting. In lithium-ion-batterijen wordt daarom ook geen puur lithium gebruikt, maar grafiet.
Terug naar Goodenough. Hij en collega’s zeggen nu wél puur lithium als anode te kunnen gebruiken. Hun elektrolyt is een glasachtige substantie die de lithiumionen door kan laten. Bij de kathode worden de lithiumionen ‘opgeslagen’ op zwavel, een stof die ook in andere batterijen wordt gebruikt.
De testbatterij werd tweehonderd keer opgeladen en ontladen, zonder een groot spanningsverlies. Dat is voor een systeem in het laboratorium respectabel. Wat betreft capaciteit gooit de batterij echt nóg hogere ogen. Ze zou zo’n 850 wattuur per kilogram kunnen opslaan. Bijna vier keer meer dan de huidige batterijen. Mogelijk een doorbraak dus, als je bedenkt dat batterijen ieder jaar gemiddeld maar zo’n vijf procent beter worden.

Veel partijen proberen betere batterij te ontwikkelen. Toyota werkt al tientallen jaren met wisselende successen aan een batterij die volledig uit vaste onderdelen bestaat.
Carlos Gomez via CC BY-NC 2.0Kritiek
Goodenough heeft een grote reputatie in het veld. Toch kwam er veel kritiek op het stuk. Collega’s uit het veld stellen dat de batterij helemaal niet kán werken. De wetten van de thermodynamica verbieden het. ‘Als iemand anders dan Goodenough dit had gepubliceerd, dan zou ik, nou, het is moeilijk om daar een net woord voor te vinden’, zei Princeton-professor Daniel Steingart in een commentaar op de website Quartz.
Ook Marnix Wagemaker, onderzoeker aan de Technische Universiteit Delft, is kritisch. “Aan de ene kant van de batterij heb je lithium, aan de andere kant heb je eigenlijk óók lithium”, zegt hij. “Normaal gesproken gebeurt er dan niets. Er gaat dan alleen een stroom lopen bij een potentiaalverschil. Theoretisch kan het als het lithium bij de kathode een positieve lading heeft. Hiervoor moet het echter worden afgeschermd van de elektrode die óók positief is.”
Volgens Wagemaker concludeert Goodenough dat de batterij werkt door het glasachtige elektrolyt. “In het artikel wordt het eigenlijk nauwelijks uitgelegd,” zegt Wagemaker, “maar er wordt gesuggereerd dat het elektrische veld van het positieve lithium wordt afgeschermd voor de rest van elektrode. Ik zie niet hoe dat werkt, aangezien het elektrolyt niet tussen het positieve lithium en de positieve elektrode zit. Er wordt hiervoor geen experimenteel bewijs geleverd.”

Het Reactor Instituut Delft, hier wordt onder andere onderzoek gedaan naar batterijen.
Nucleair NederlandElektrolyt opeten
In Delft proberen onderzoekers nu te kijken wat er precies gebeurt in de batterij van Goodenough. “Ik denk dat wij met onze meettechnieken, waarmee we op atomaire schaal kunnen zien, een beter begrip krijgen van wat er hier met het lithium gebeurt”, zegt Wagemaker. “Eigenlijk is dat iets wat Goodenough en collega’s zelf hadden moeten doen. Ik denk ook dat iedere andere wetenschapper was afgerekend op het feit dat ze daar niet verder naar gekeken hebben, maar Goodenough blijkbaar niet.”
Peter Notten, hoogleraar Energy Materials and Devices aan de Technische Universiteit Eindhoven, sluit zich aan bij de kritiek. ‘De verklaring die ze voor de werking van de kathode presenteren kan ik moeilijk doorgronden en geloven’, laat hij per mail weten. ‘Anderen hebben gewezen op een mogelijk nevenreactie met zuurstof, die de spanning verklaart. Maar waar komt die zuurstof vandaan in deze gesloten batterij?’
Spectaculaire nieuwe vindingen in het batterijenveld bleken al vaker te mooi waren om waar te zijn. Wagemaker wijst op ongewenste chemische reacties in het elektrolyt. “Je bent dan je elektrolyt aan het ‘opeten’. Omdat je in een commerciële batterij zo weinig mogelijk elektrolyt hebt, krijg je daar nauwelijks spanning”, zegt hij.
Wagemaker zegt dat het batterij-onderzoeksveld wordt ‘geteisterd’ door hypes, en dat zich dat uiteindelijk tegen het onderzoek keert. “Ik snap het wel, er is maar een beperkte hoeveelheid geld beschikbaar voor onderzoek en iedereen probeert zoveel mogelijk financiering binnen te halen. Artikelen in gerenommeerde tijdschriften helpen daarbij. Maar als je tien keer iets belooft en het blijkt telkens te mooi om waar te zijn, dan gelooft uiteindelijk niemand je meer.”

