Medicatie bij de ziekte van Alzheimer is vooral gericht op symptoombestrijding. Kan dat niet anders, vroegen wetenschappers van de Universiteit Twente zich af. De komende vier jaar gaan zij proberen een cocktail van medicijnen met behulp van nanodeeltjes gericht in de hersenen te brengen.
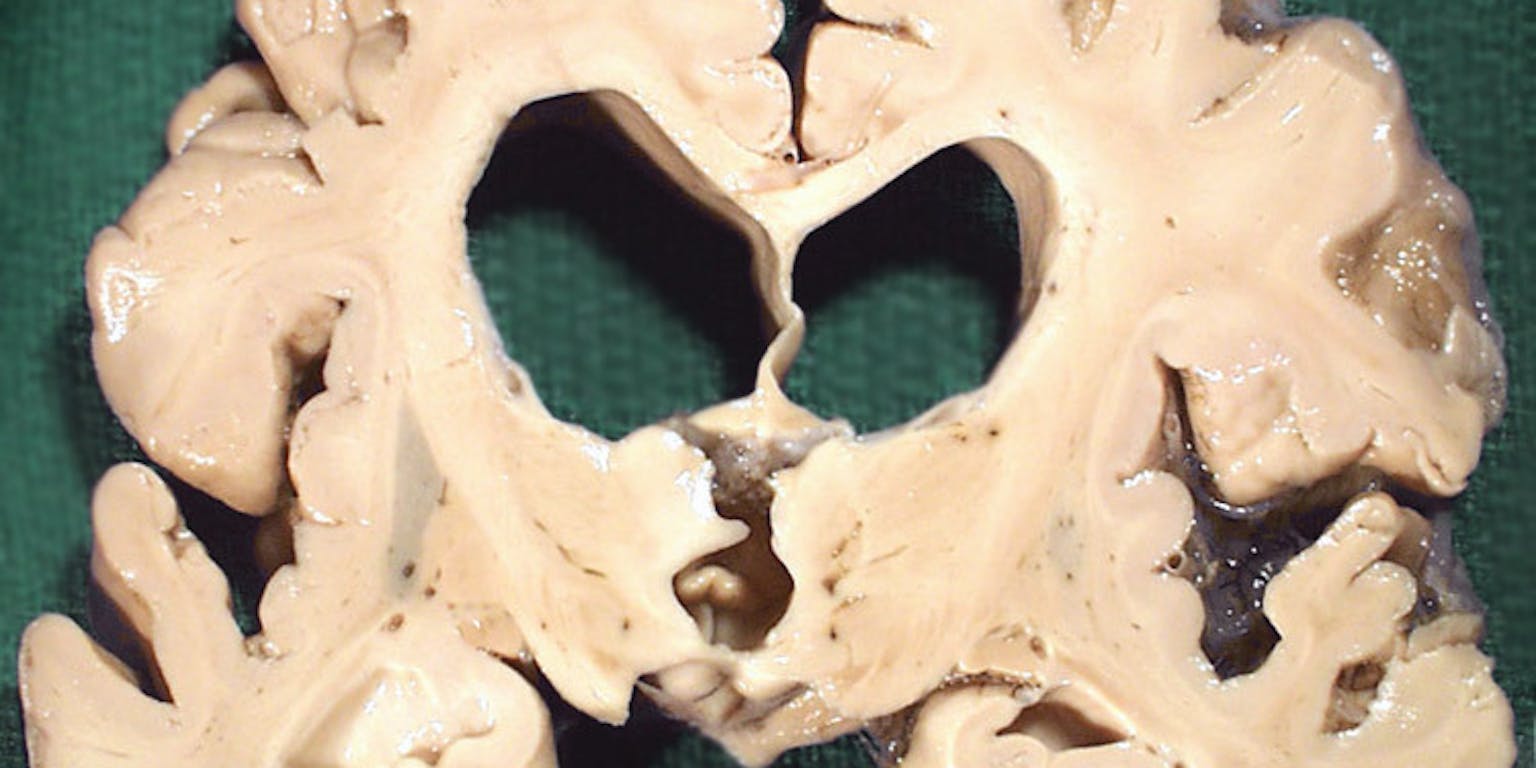
De ziekte van Alzheimer is een vorm van dementie, waarbij het eiwit amyloïd bèta in de hersenen onvoldoende wordt afgebroken. Overtollig eiwit klontert samen tussen de zenuwcellen, waardoor deze kapot gaan. Met geheugenstoornissen, taalstoornissen en stemmingsveranderingen tot gevolg. Alzheimer is een complexe ziekte en is niet te genezen. Behandeling richt zich meestal op het onderdrukken van de symptomen. Zo zijn er medicijnen die de verslechtering van het geheugen vertragen en medicijnen die probleemgedrag, zoals onrust of agressie, bestrijden.
‘Multipil’
Dat de behandeling van Alzheimer beperkt blijft tot symptoombestrijding is volgens nanobyofysica Kerensa Broersen (Universiteit Twente) te wijten aan het feit dat de huidige medicijnen de complexiteit van de ziekte onderschatten. “Die medicijnen focussen op één enkele factor van de ziekte en proberen die te onderdrukken”, zegt zij. “Wij willen een ‘multipil’ ontwikkelen, waarbij we rekening kunnen houden met verschillende factoren.” De komende vier jaar gaan Broersen en haar collega’s, in samenwerking met verschillende partners, onderzoeken of zo’n multipil een concept kan zijn voor de behandeling van Alzheimer. Zij kregen daarvoor een subsidie van bijna 900.000 euro binnen het Deltaplan Dementie van ZonMW, de Nederlandse organisatie voor gezondheidsonderzoek en zorginnovatie.
De multipil zal een cocktail van medicijnen bevatten en moet de hersenen binnen kunnen komen, ongeacht wat erin zit. Broersen zelf houdt zich met name bezig met dat eerste aspect; het ontwerpen van de medicijncocktail. “Daarvoor gebruiken we deels bestaande medicijnen die zich, zoals gezegd, specifiek richten op een onderdeel van de ziekte”, vertelt ze. “Daarnaast werken we samen met het bedrijf Crossbeta Biosciences. waar ze honderdvijftig kandidaatmedicijnen klaar hebben liggen. Met behulp van fluorescentie kunnen we bepalen welke van deze kandidaatmedicijnen het beste in staat zijn om de giftigheid van de eiwitklontjes te neutraliseren. In totaal hebben we de keuze uit ongeveer tweehonderd medicijnen, waarvan er uiteindelijk vier in de cocktail terecht moeten komen.”
Barrière
Geen gemakkelijke selectie dus. Temeer omdat er nog veel vragen onbeantwoord zijn. Broersen: “We weten dat er bij patiënten met de ziekte van Alzheimer vaak meer van het eiwit amyloïd bèta in de hersenen aanwezig is dan bij gezonde mensen. We willen de afbraak van dat eiwit dus een boost geven. Maar welke enzymen breken dit eiwit af? Hoe gebeurt dat precies? En kunnen de fragmenten die je na afbraak overhoudt ook weer samenklonteren? Dat zijn allemaal dingen die we nog niet weten.”
Voor Broersen is het onderzoeksproject geslaagd als de ontwikkelde medicijncocktail het uiteindelijk beter blijkt te doen dan losse medicijnen tegen Alzheimer. Om dat voor elkaar te krijgen, moet de multipil terecht komen in de hersenen en meer specifiek; in de hippocampus. “Dit is het gebied van cognitie, waarneming en herinneringen. Daar begint de afzetting van het eiwit en de afbraak van zenuwcellen”, vertelt Broersen. Het probleem is dat de hersenen helemaal niet efficiënt zijn in het opnemen van medicijnen. Een medicijn dat op de hersenen werkt, komt momenteel voor ongeveer 1 procent terecht op de plaats van bestemming. De overige 99 procent verdwijnt elders in het lichaam.
De hersenen hebben dan ook een fantastisch systeem om alles dat lichaamsvreemd is buiten de deur te houden; de bloed-hersen barrière. Broersen: “Die barrière is selectief op grootte van deeltjes. Deeltjes die te groot zijn, krijgen een soort vlaggen opgeplakt en worden daardoor herkend. Wij willen heel kleine deeltjes maken, die makkelijker naar binnen glippen.” Die deeltjes zouden de medicijncocktail naar de hersenen kunnen vervoeren.
Slapeloze nachten
Jos Paulusse, biomedisch chemicus aan de Universiteit Twente, buigt zich de komende jaren over het maken van die kleine deeltjes. “We willen ze nog een stuk kleiner maken dan de standaard nanodeeltjes zoals we die nu kennen”, vertelt hij. “Nanodeeltjes van ongeveer honderd nanometer groot zijn gebruikelijk, de nieuwe deeltjes worden niet groter dan tien tot vijftien nanometer. Ze worden gemaakt door polymeren op te rollen. Voorheen plakten onderzoekers hiervoor een aantal polymeren aan elkaar, maar wij creëren nu van één polymeer één nanodeeltje.” De lengte van een polymeer bepaalt hoe groot een deeltje wordt. Dus door een minder lange ketting van polymeren te gebruiken, worden de deeltjes vanzelf kleiner.
Het wordt waarschijnlijk een grote uitdaging om de geselecteerde medicijnen uiteindelijk in de gemaakte nanodeeltjes te stoppen. Paulusse: “Bij de kandidaatmedicijnen zitten kleine moleculen waarvan ik het idee heb dat het wel gaat lukken om ze in een nanodeeltje te krijgen. Maar er zijn ook enzymen en eiwitten, behoorlijk complexe moleculen die je niet zo makkelijk in een deeltje kunt stoppen. Dat wordt dus al lastiger. En of we actieve enzymen in een nanodeeltje krijgen? Dat is een vraag waar ik nu al slapeloze nachten van heb. Voor mij is het project geslaagd bij succesvolle medicijnafgifte in de hersenen, maar de hele cocktail aan medicijnen afleveren zou natuurlijk fantastisch zijn.”
Utopie
Mocht dit systeem werken, dan biedt dat de mogelijkheid om in een heel vroeg stadium ziektes aan te pakken. Niet alleen de ziekte van Alzheimer, maar mogelijk ook andere complexe hersenziekten zoals de ziekte van Parkinson. “Symptoombestrijding is er al. Wij willen nu een stap verder gaan door het verlies van zenuwcellen te remmen”, zegt Broersen. “De ziekte genezen op het moment dat de zenuwcellen al verloren zijn gegaan, gaat heel moeilijk worden. De hersenen maken vrij weinig nieuwe zenuwcellen aan. En zelfs al zouden ze dat wel doen; herinneringen die verloren zijn gegaan krijg je niet zomaar meer terug. Dat is echt een utopie.”