De hele wereld gaat digitaal. Op steeds meer plekken wordt er gewerkt met razendsnelle computers en andere slimme apparatuur. Maar niet op de pathologieafdeling van een ziekenhuis. De patholoog typt zijn verslag op de computer, maar verder is zijn bureau gevuld met een microscoop en vele microscoopglaasjes met preparaten die bekeken moeten worden.
Pathologie speelt een cruciale rol in het bepalen van het ziektebeeld, met name bij diagnose van kanker. Verdachte weefselmonsters worden met een microscoop onderzocht om te bepalen of het tumorweefsel kwaadaardig is. Aan de hand daarvan brengt de patholoog advies uit over de behandeling van de patiënt.
“De microscoop blijft natuurlijk een fantastisch apparaat, maar er zitten nadelen aan de logistiek van preparaten op glas”, vertelt Dirk Verhagen, onderzoeker en ontwikkelaar bij Philips. “Je kunt beelden kwijt raken, bijvoorbeeld doordat glaasjes breken of doordat je het preparaat doorstuurt naar een specialist voor een consult.” Om de opslag en het delen van pathologische beelden makkelijker te maken, ontwikkelde Philips als onderdeel van het Cyttron II-onderzoeksprogramma de IntelliSite digitale pathologie-oplossing. Het systeem bestaat uit een glaasjesscanner, een beeldbeheersysteem en software waarmee de patholoog de beelden kan delen en beoordelen.

De snelheid van pathologiescanners is enorm toegenomen. De eerste scanners deden een halfuur over één microscoopglaasje. Nu worden driehonderd glaasjes binnen vijf tot acht uur verwerkt.
PhilipsBehoorlijke datavolumes
In het bezoekerscentrum in Best demonstreert Verhagen hoe het systeem werkt. Hij plaatst een microscoopglaasje in de scanner, doet de deur dicht en drukt op ‘start’. Ongeveer een minuut later is de scan klaar. De eerste scanners deden een halfuur over zo’n glaasje. Deze scanner kan driehonderd glaasjes in vijf tot acht uur verwerken. “Dat maakt dat scannen aantrekkelijk is geworden voor pathologisch onderzoek”, vindt Verhagen.
Niet alleen de duur van het scannen is flink naar beneden gebracht, ook de opslag van de beelden die eruit rollen is nu betaalbaar. “Afhankelijk van wat je precies scant, komen er databestanden uit variërend van 0,5 tot 4 of 5 gigabyte (GB). Dat zijn behoorlijke datavolumes, die je allemaal ergens moet opslaan. Dat kan nu voor een redelijke prijs. Soms is het zelfs al goedkoper dan het opslaan van microscoopglaasjes in een archief, zoals nu gebeurt”, vertelt Verhagen.
‘Bladeren’ door weefsel
Imagingspecialist Jelte Vink van Philips was verantwoordelijk voor de ontwikkelingen aan het digitale pathologiesysteem. “Het apparaat was er al. Wat we de afgelopen vier jaar met name gedaan hebben, zijn updates van de software waardoor het mogelijk wordt om beelden naast elkaar te leggen of op dezelfde plek in een preparaat naar verschillende kleuringen te kijken”, legt hij uit.
Verhagen kan dit direct demonstreren met beelden die eerder op de computer zijn opgeslagen. Stel; de arts heeft een stukje weefsel weggenomen bij een patiënt en wil graag weten of het een tumor is en hoe die tumor dan groeit. De patholoog maakt hele dunne plakjes van het weggenomen weefsel en prepareert die allemaal op een eigen glaasje. Door de glaasjes één voor één te bekijken, valt iets te zeggen over de locatie van de tumor. Bijvoorbeeld of hij oppervlakkig zit of juist diep in het weefsel.

Het IntelliSite systeem van Philips bestaat uit een glaasjesscanner (links), een beeldbeheersysteem en software.
Philips“Na het scannen van de glaasjes kun je beelden naast elkaar leggen en ook aan elkaar linken”, legt Verhagen uit. “Virtueel kun je de verschillende plakjes dus weer op elkaar leggen en zo als het ware door het weefsel heen ‘bladeren’. Dan kun je met veel grotere precisie zeggen hoe een tumor bijvoorbeeld in de diepte groeit.”
Gevoelige tumorcellen
Bij het prepareren van microscoopglaasjes krijgt ieder plakje weefsel zijn eigen kleuring. En met iedere kleuring kun je verschillende dingen aantonen. Met de computer kun je nu heel precies twee verschillende kleuringen van hetzelfde gebied naast elkaar leggen. Verhagen laat het zien. Op het eerste glaasje zijn de celranden aangekleurd met roze en de celkernen met blauw-paars. “Met zo’n kleuring kun je zien of je te maken hebt met kanker”, vertelt hij. “Het weefsel ligt dan niet mooi geordend, maar toont een wildgroei van cellen. Gebieden die helemaal blauw-paars lijken te kleuren, markeren het tumorweefsel.”
Op het tweede glaasje is een bruine kleuring gebruikt, die aangeeft of een patiënt ontvankelijk is voor hormoonbehandeling. Wat je aan dit voorbeeld ziet, is dat de gebieden die op het eerste glaasje blauw-paars kleurden op het tweede glaasje bruin kleuren. Dat betekent dat deze patiënt tumorcellen heeft die ontvankelijk zijn voor hormoonbehandeling. Verhagen: “Dat is belangrijk om te weten, want dergelijke chemotherapie (bijvoorbeeld het medicijn Herceptin) kan consequenties hebben voor het functioneren van het hart. Dus dat wil je niet zomaar geven aan een patiënt die het niet nodig heeft.”
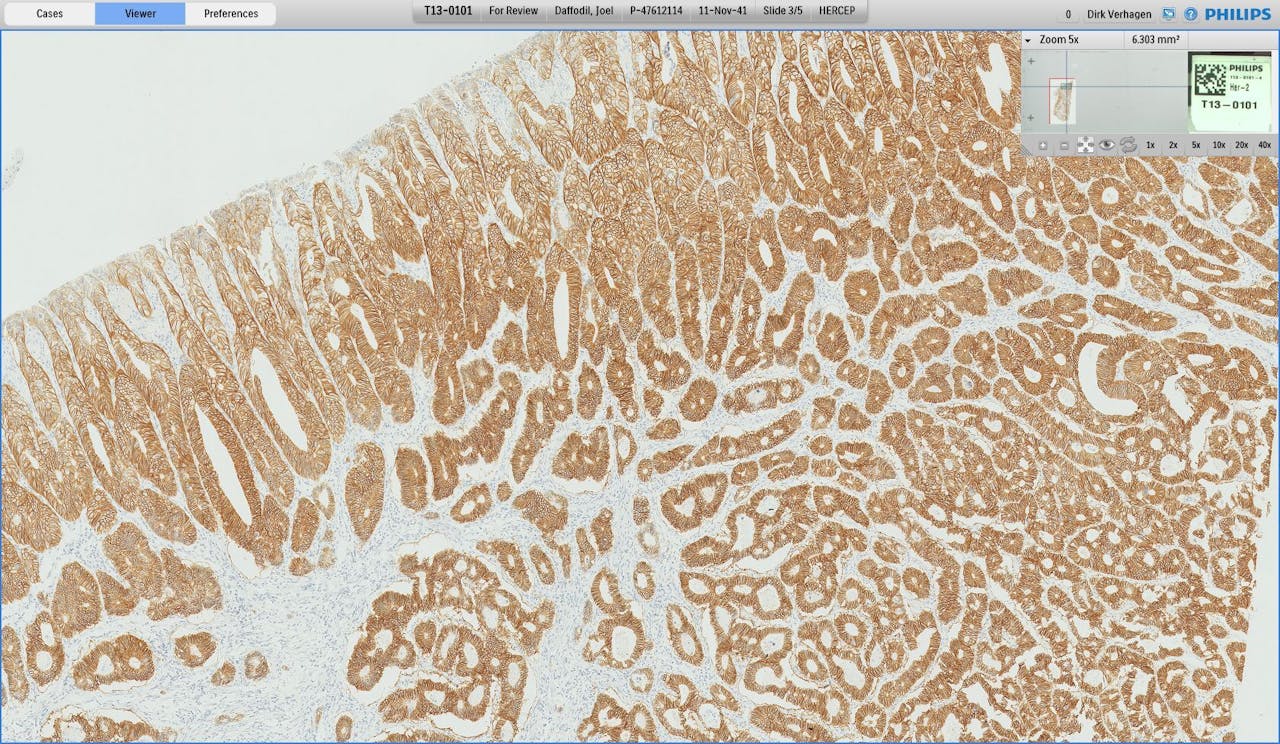
Screenshot van een Herceptinkleuring. Door dit plaatje naast een standaard celkleuring te leggen, kan een patholoog direct zien of de tumorcellen van een patiënt ontvankelijk zijn voor hormoonbehandeling.
Philips IntelliSite Pathologist SuiteBeelden sorteren
Met het digitale pathologiesysteem kan nu al meer dan met een traditionele microscoop alleen, maar het apparaat moet in de toekomst nog veel slimmer worden. Onderzoekers zijn hard bezig om honderdduizenden oude microscoopglaasjes uit archieven te digitaliseren. “We weten al wat er met die patiënten is gebeurd en daar kunnen computers van leren”, legt Verhagen uit. “Misschien is het wel zo dat het vetweefsel bij een bepaald type tumor anders groeit. De patholoog heeft daar waarschijnlijk nooit zo naar gekeken omdat hij geen voorbeelden van hetzelfde tumortype uit het archief kan halen om ze naast elkaar te onderzoeken.”
Ook kan de computer het werk van de patholoog makkelijker maken. Bijvoorbeeld bij het zoeken naar uitzaaiingen. Verhagen: “De patholoog verwijdert een stukje van een lymfeklier en maakt daar tien tot vijftig glaasjes van. Die kun je allemaal bekijken, maar één treffer is in principe voldoende om aan te tonen dat er uitzaaiingen zijn. Wat de computer kan doen, is een voorselectie maken van de beelden zodat de patholoog de meest ‘verdachte’ beelden het eerst te zien krijgt.”

