Vanaf eind dit jaar mogen alleen tandartsen nog tandbleekmiddelen met een hoge concentratie waterstofperoxide gebruiken. Bij de drogist of schoonheidssalon kun je zulke producten straks niet meer krijgen. Is het bleken van je gebit dan zo slecht? Wat zijn de gezondheidsrisico’s van waterstofperoxide in je mond?
Tanden zijn van nature niet wit, maar een beetje gelig. Naarmate je ouder wordt hopen kleurstoffen uit je voeding zich op in je tanden waardoor ze geler worden.
Flickr, Christian Aagaard via CC0In Hollywoodfilms en reclames zie je niet anders: filmsterren en andere beroemdheden die met hun spierwitte glimlach van het witte doek spatten. En ook in Nederlandse tijdschriften en televisieprogramma’s lachen stralend witte tanden ons toe. Een wit gebit, wie wil het niet? Maar het bleken van tanden is niet zonder risico.
Tot nu toe was er door de Nederlandse Voedsel- en Warenautoriteit (VWA) geen limiet gesteld aan het waterstofperoxidegehalte in de bleekmiddelen die tandartsen gebruiken. Maar vanaf 1 november 2012 mogen tandartspraktijken in Nederland en in de rest van Europa geen bleekmiddelen meer gebruiken met meer dan zes procent waterstofperoxide.
Volgens de NOS zijn er op dit moment gespecialiseerde klinieken die bleekmiddelen verhandelen met 15, 25 of zelfs 35 procent waterstofperoxide. Drogisterijen, schoonheidssalons en mondhygiënisten mogen alleen nog tandbleekmiddelen verkopen met minder dan 0.1% waterstofperoxide. Vanwaar deze strenge eisen? Is het gebruik van waterstofperoxide dan zo slecht voor je tanden en mond?
Whitening tandpasta
Waterstofperoxide is een kleurloze vloeistof met een bittere smaak die goed oplost in water. Dat klinkt onschuldig, maar het is geen kinderachtig middeltje. Het agressieve zit hem in de oxiderende werking. Waterstofperoxide werkt als oxidator, wat betekent dat het in een chemische reactie elektronen opneemt van een andere stof die daardoor andere eigenschappen krijgt (zoals kleur of geur).
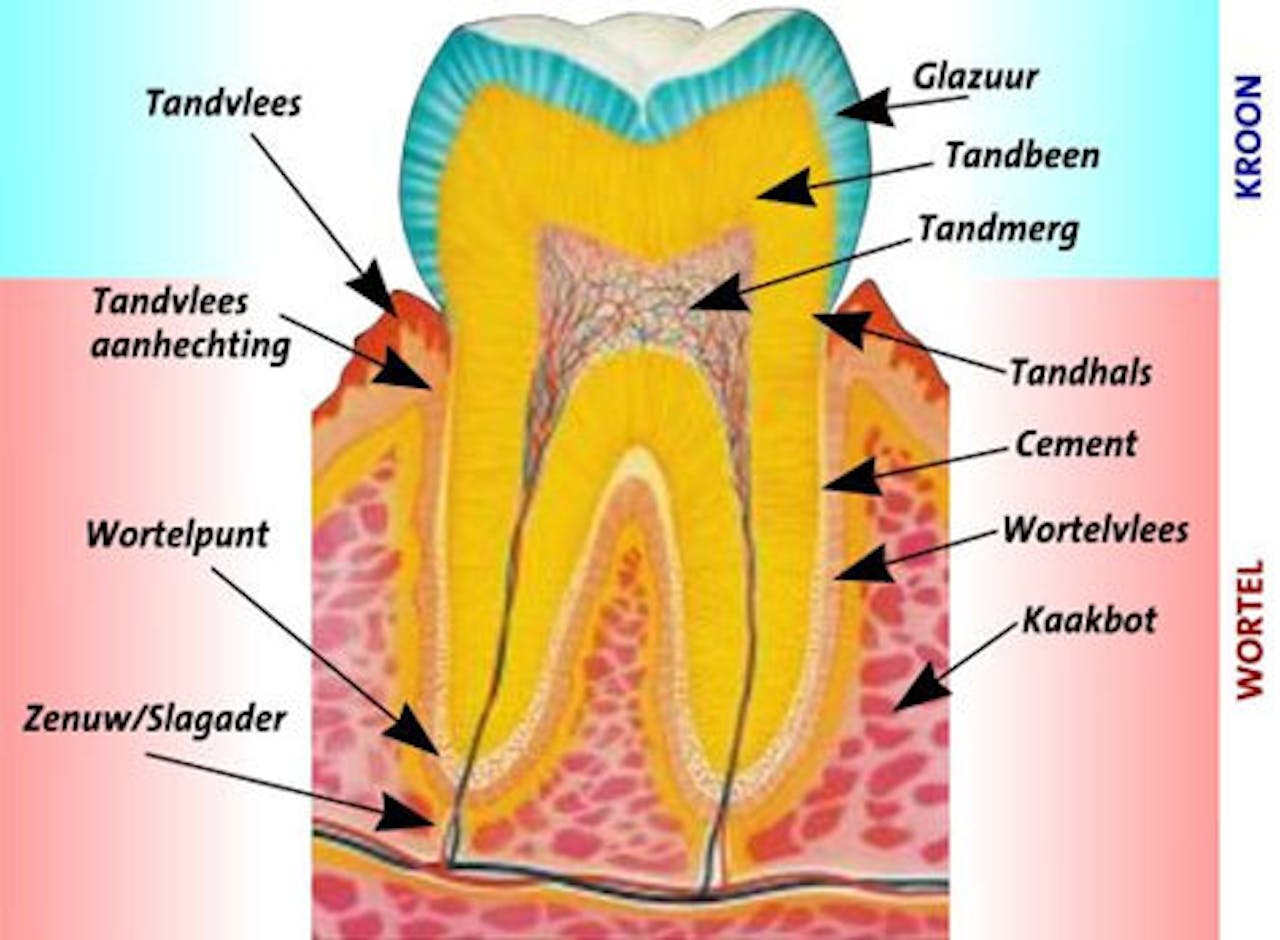
Bij het aanbrengen van een bleekgel dringt het waterstofperoxide via het tandglazuur door tot in het binnenste van de tand, het tandbeen.
Daar bindt het aan de pigmenten die verkleuringen van het tandbeen veroorzaken. Waterstofperoxide valt de chemische verbindingen aan waar het pigment uit bestaat waardoor deze kleurmoleculen omgezet worden in kleuloze restproducten.
Om tanden te witten bestaan er ook producten waar geen waterstofperoxide inzit. In veel whitening tandpasta’s bijvoorbeeld zit zuiveringszout dat de donkere aanslag aanpakt die ontstaat door roken en het drinken van koffie en thee. Maar tegen gele tanden doet zo’n tandpasta weinig. Om gele tanden witter te maken werken alleen bleekmiddelen met waterstofperoxide of carbamide-peroxide – een chemische stof samengesteld uit ureum en waterstofperoxide waaruit het reactieve waterstofperoxide kan vrijkomen.
Dodelijke dosis
De laatste tien jaar zijn zijn de gezondheidsrisico’s van waterstofperoxide en carbamide-peroxide voor het bleken van tanden uitvoerig onderzocht. Zo is er onderzoek gedaan naar het inslikken van waterstofperoxide, irritatie aan de slijmvliezen in de mond en de huid, beschadiging van de tanden en zelfs of waterstofperoxide kanker kan veroorzaken. Een hele klus, want het is lastig om vast te stellen met hoeveel waterstofperoxide iemand in aanraking komt tijdens het tanden bleken. Dat hangt af van de manier van bleken en van de concentratie waterstofperoxide in het bleekmiddel.
Waterstofperoxide kan in grote hoeveelheden zeer gevaarlijk zijn als je het inslikt. Er zijn gevallen bekend van mensen die overleden nadat ze een te grote dosis waterstofperoxide binnenkregen. Zo overleed in 1994 een eenjarig jongetje nadat hij per ongeluk een fles met drie procent waterstofperoxide had opgedronken. Hij kreeg in totaal zeven gram binnen. Dat is veel voor een lichaamsgewicht van elf kilo. Ook uit diertesten blijkt dat de helft van de ratten het loodje legt als ze per kilogram lichaamsgewicht één gram waterstofperoxide binnen krijgen.
Maar met tandbleekmiddelen kom je bij lange na niet in aanraking met zulke grote hoeveelheden waterstofperoxide, laat staan dat je alles doorslikt. Naar schatting slik je 25 procent van de waterstofperoxide in die is aangebracht voor het bleken. Daar kan je in het ergste geval diarree van krijgen, maar je zult er niet dood aan gaan.
En hoe zit het met kanker? Er zijn aanwijzingen uit proefdieronderzoek dat waterstofperoxide de groei van kankercellen kan versnellen in dieren die het spul te drinken kregen. Maar dat waterstofperoxide in tandbleekmiddelen kanker kan veroorzaken is nog nooit aangetoond in mensen.

In sommige whitening tandpasta’s zit waterstofperoxide. Maar dat is zo weinig dat je tanden er eigenlijk niet echt witter van worden.
thegreenj | wikimedia commonsTandvleesirritatie
Tandbleekmiddelen met waterstofperoxide treffen dus niet het lichaam als geheel – zelfs niet als je ze inslikt. Bovendien wordt het goedje razendsnel afgebroken. Maar waterstofperoxide kan plaatselijk in de mond wel wat narigheden veroorzaken. Bij gebruik van bleekmiddelen met meer dan 6 procent waterstofperoxide kan het tandvlees tijdelijk geïrriteerd raken. Ook kunnen de tanden overgevoelig worden voor koud en warm eten en drinken doordat het tandglazuur poreuzer wordt.
Maar bij een gehalte waterstofperoxide lager dan 6 procent zijn die risico’s er niet, volgens een rapport van Scientific Committee on Consumer Safety van de EU. Mits de tandbleekmiddelen goed gebruikt worden. En dat is op dit moment niet altijd het geval omdat ook schoonheidssalons en mondhygiënisten die niet gespecialiseerd zijn ook mogen bleken met hoge concentraties waterstofperoxide. Dan kan er best iets mis gaan. Als het bitje waarin de bleekgel zit niet goed past bijvoorbeeld, kan er waterstofperoxide op je tandvlees terechtkomen met vervelende kleine witte brandwondjes tot gevolg. En voor sommige mensen is het sowieso onverstandig om te bleken, vanwege blootliggend tandbeen of slecht aansluitende vullingen. Dan is het niet verwonderlijk dat het goedje gaat irriteren. Of iemand geschikt is, is aan een deskundige om te bepalen.
De VWA wil met zijn strengere eisen dus naast het indammen van gezondheidsrisico’s ook het onjuist gebruik van tandbleekmiddelen een halt toe roepen. Vandaar dat bleken met meer dan 0.1 procent waterstofperoxide straks alleen mogelijk wordt bij tussenkomst van een tandarts.