Een recente techniek, waarbij specifieke cellen in het brein door designerdrugs extra actief worden, helpt onderzoek naar psychiatrische ziekten. Dat laat neurobioloog Linde Boekhoudt zien aan de hand van studies met ratten. Ze promoveerde deze week aan de Universiteit Utrecht.
Nieuwe doelgerichte behandelingen voor psychiatrische stoornissen laten op zich wachten, omdat het moeilijk is om te ontleden welk stukje brein verantwoordelijk is voor welk gedrag. Waar in de hersenen komen de overdreven reacties op onbelangrijke gebeurtenissen vandaan, zoals het geval is bij schizofrenie? En welke neurale netwerken liggen ten grondslag aan de hyperactiviteit bij ADHD?
Een technologie die selectief delen van het brein actiever maakt, kan een tipje van de sluier oplichten. Dat blijkt uit het promotieonderzoek van neurobioloog Linde Boekhoudt, verbonden aan het Universiteit Medisch Centrum Utrecht. In de nieuwe techniek worden specifieke hersencellen voorzien van een nieuw eiwit. De cellen worden geactiveerd als de bijpassende designerdrug aan dat eiwit (receptor) bindt.
Slot en sleutel
Lichaamscellen maken voor communicatie veelvuldig gebruik van receptoren op het celoppervlak, waar stoffen als hormonen en andere eiwitten aan binden. Zo’n stof hecht alleen aan een bijpassende receptor, net zoals een sleutel maar op één slot past. Binding maakt de receptor actief, waardoor er signalen de cel in gestuurd worden. Die signalen vertellen de cel bijvoorbeeld harder of minder hard te werken.
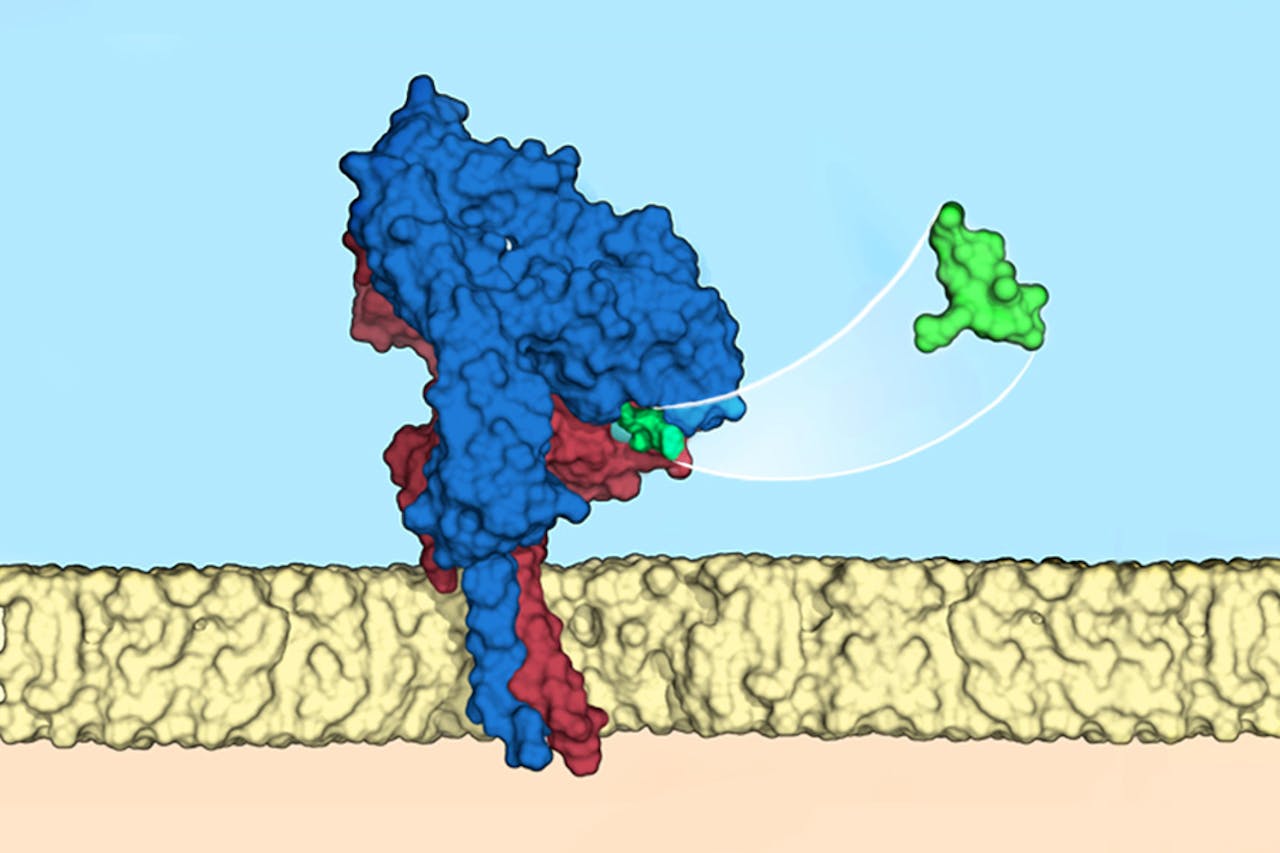
Een voorbeeld van een receptor op het celoppervlak (blauw) waar een stof (groen) aan bindt.
Francesco S. di Leva, Luciana Marinelli / Università di Napoli Federico IIDe nieuwe technologie werkt volgens hetzelfde sleutel-slot-principe, maar dan met in het lab aangepaste onderdelen die oorspronkelijk niet in het lichaam voorkomen. Het wordt gebruikt in experimenten met ratten. Het dier krijgt eerst een onschadelijk virus ingespoten dat als koeriersdienst de nieuwe receptor aflevert in zenuwcellen waarin onderzoekers geïnteresseerd zijn. Op deze receptor past één sleutel: een drug uit het lab. Zonder dit middel doet de receptor niks. Maar geef de dieren een injectie met de drug en hun hersencellen met de receptor worden tijdelijk extra actief.
“Deze zogenaamde DREADD-technologie (designer receptors exclusively activated by designer drugs) helpt ontrafelen hoe neurale netwerken het gedrag sturen”, vertelt Boekhoudt. “Het is een mooie techniek voor dieronderzoek.”
Gedragsverandering
Zelf bekeek de Utrechtse promovenda hoe dopamine producerende zenuwcellen gedrag beïnvloeden. Deze cellen zitten in de middenhersenen en verspreiden dopamine – essentieel voor beweging, eetgedrag, motivatie en aandacht – door het hele brein. Veel psychiatrische stoornissen zoals schizofrenie, ADHD, verslaving en depressie hangen samen met veranderingen in dopamine. Het fijne is er niet van bekend. “We weten bijvoorbeeld niet of er in het geval van ADHD juist te veel of te weinig dopamine is”, legt Boekhoudt uit. Daarnaast is het onduidelijk in welke mate veranderde activiteit van dopaminecellen daadwerkelijk leidt tot een gedragsverandering.
In haar experimenten maakte ze dopaminecellen in het brein van ratten tijdelijk extra actief. “De cellen gaan dan meer vuren, waardoor er meer dopamine wordt afgegeven”, legt Boekhoudt uit. Een half uur na injectie met het middel veranderde het gedrag van de ratten: ze werden onder meer hyperactief en snel afgeleid. Activatie van de dopaminecellen geeft de dieren een soort ‘gaan-signaal’, denkt Boekhoudt.
Abnormale hersenactiviteit
In de toekomst wordt DREADD wellicht meer dan een onderzoekstool. Boekhoudt verwacht dat de technologie op den duur doelgericht verstoorde hersenactiviteit in patiënten kan behandelen. “Dat gebeurt nu met medicijnen als antipsychotica en Ritalin, maar die middelen grijpen pas in nadat dopamine al is vrijgegeven”, zegt Boekhoudt. Met DREADD kan je voorkomen dat die afgifte plaatsvindt, bij aandoeningen waarin een teveel aan dopamine het probleem is.
Om de techniek toe te passen in de kliniek moet je wel weten waar de abnormale hersenactiviteit zit in het brein. Epilepsie heeft volgens Boekhoudt de meeste potentie om met DREADD behandeld te worden. “Bij epilepsie is goed te lokaliseren waar de aanvallen zich voordoen, die gebeuren doorgaans heel geconcentreerd. Op die plek zou je gericht het virus kunnen inspuiten dat de receptor aflevert. Maar zover zijn we nog lang niet.”