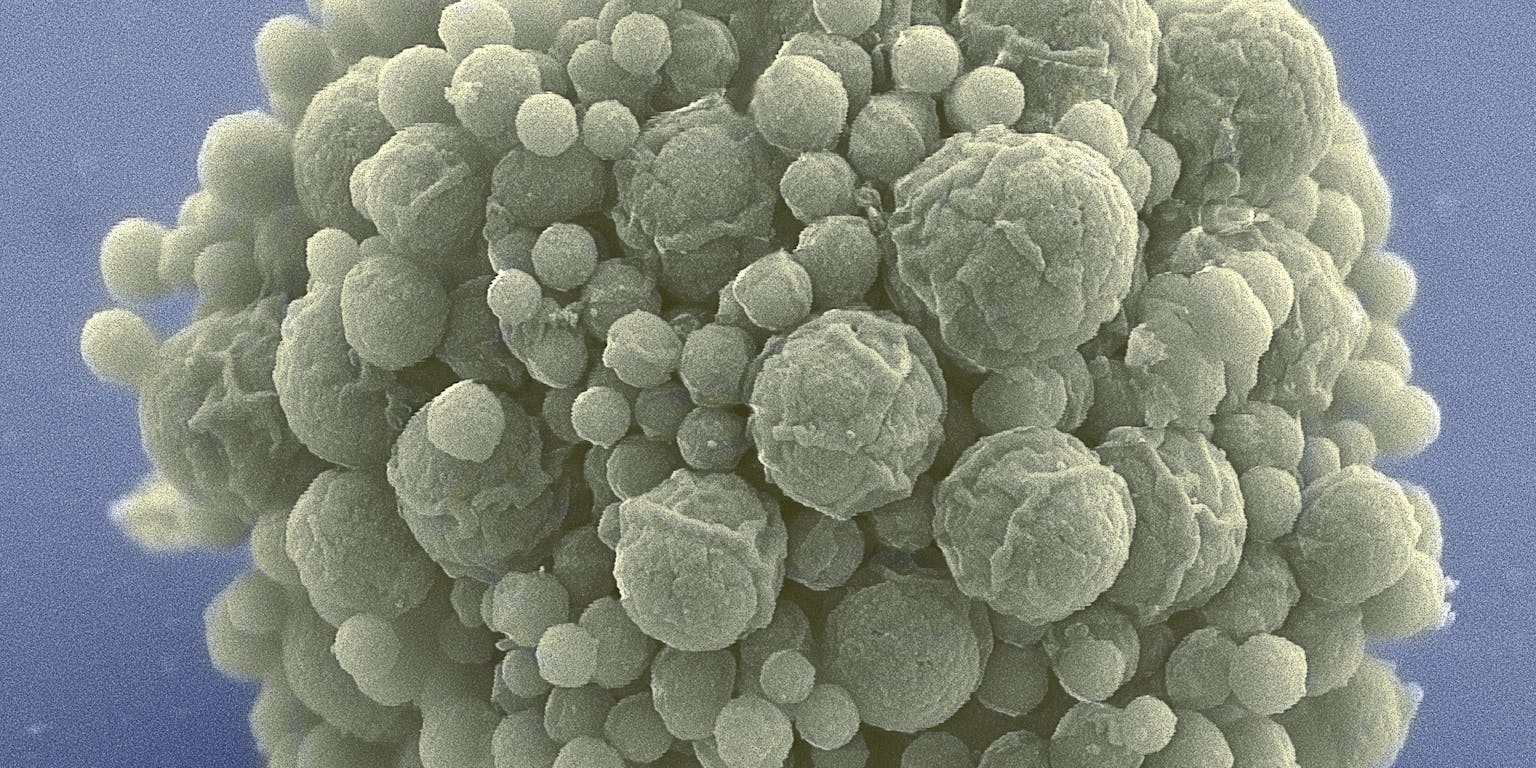
Bacterie JCVI-syn3.0 is de nieuwe lichtgewicht kampioen: van alle levende cellen die we nu kennen heeft deze ‘designbacterie’ het kleinste aantal genen. In Science publiceerden de Amerikaanse makers hoe ze hun bacterie hebben gemaakt. Het meest opvallende resultaat: van een derde van de cruciale genen weten we eigenlijk helemaal niet wat ze doen.
Bestaat er zoiets als een minimaal genoom? Een verzameling genen die stuk voor stuk cruciaal zijn voor leven? De genen die zelfs de meeste simpele levensvorm nodig heeft? En als we weten welke genen dat zijn, kunnen we dan zo’n genoom maken en zorgen dat het werkt?
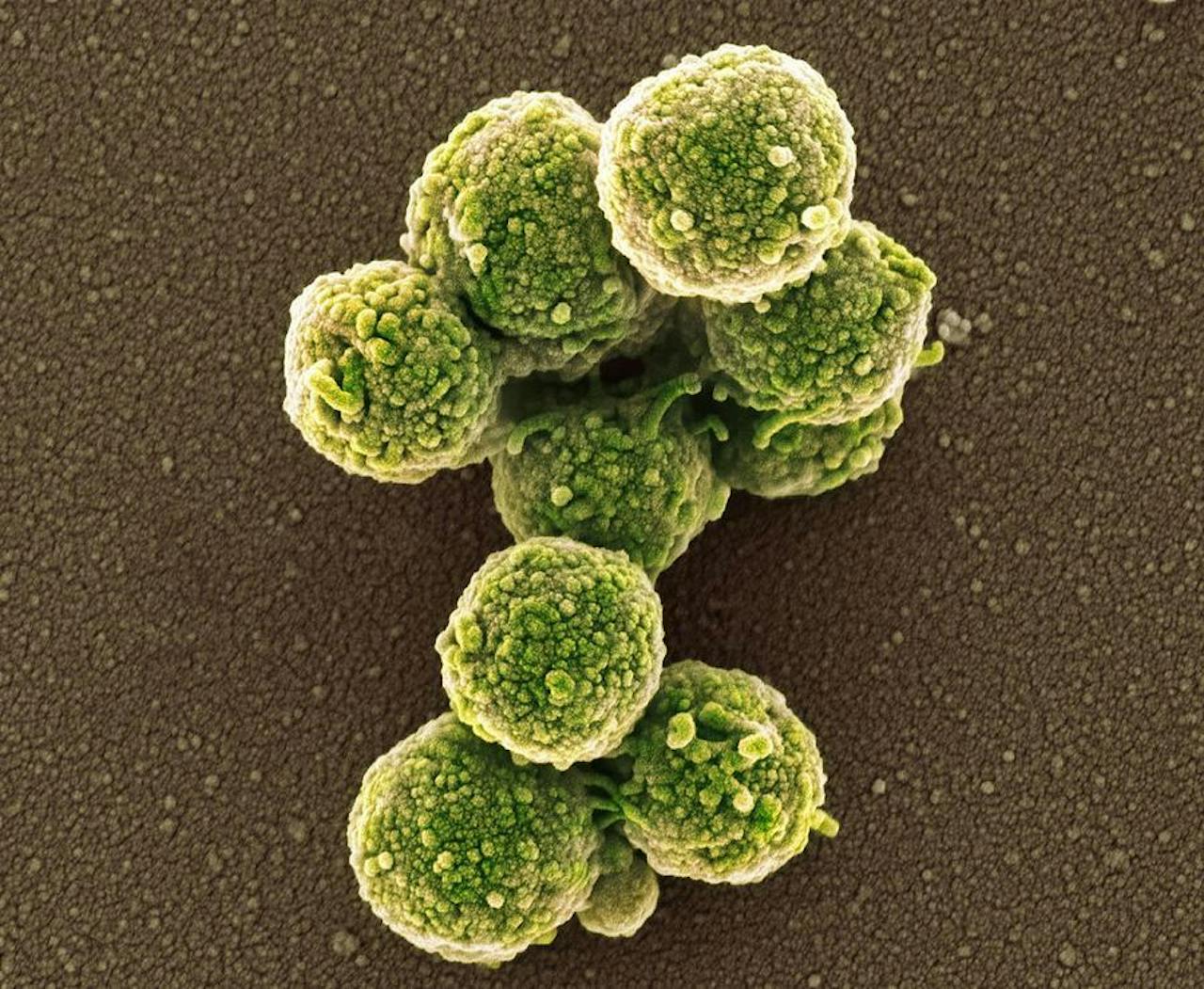
Opname van JCVI-syn1.0, de eerste levende bacterie met een volledig synthetisch genoom, gemaakt in 2010.
Tom Deerinck/NCIMR/UCSDIn 2010 kregen we een positief antwoord op die laatste vraag. De Amerikaanse genoomonderzoeker/-ondernemer J. Craig Venter en zijn team publiceerden toen de eerste levende bacterie met een volledig synthetisch genoom: JCVI-syn1.0. Ze hadden alle genetische informatie uit de bacterie Mycoplasma capricolum gehaald. In die lege huls plaatsten ze vervolgens een nieuw genoom, dat ze helemaal vanaf nul hadden opgebouwd in het lab.
Voor dit synthetische genoom hadden ze als voorbeeld het genoom van een andere bacterie, Mycoplasma mycoides, gebruikt; en het werkte. De combinatiebacterie JCVI-syn1.0 leefde en produceerde alle eiwitten die M. mycoides normaal ook maakt. Bovendien kon de synthetische bacterie zich delen, waarmee helemaal sprake was van een levende cel.
Helft eruit
Het genoom van de Mycoplasma-bacteriën behoort tot de kleinste genomen van alle zelfstandig delende organismen die we tot nu toe kennen. Maar is het ook het kleinst mogelijke genoom? Of kan er nog wel wat uit? Om dat uit te zoeken keken Venter en collega’s kritisch naar de genetische informatie van JCVI-syn1.0 en begonnen ze stapsgewijs genen en gebieden in het genoom te verstoren om te zien of dat een effect had. Al snel bleek dat grofweg de helft van de genen zonder problemen naar de vuilnisbak kon.
Na nog wat preciezer zoeken, proberen en soms weer terugplaatsen van een gen, bleef uiteindelijk JCVI-syn3.0 over. Een levende bacterie met slechts 473 genen. Ter vergelijking: de bekende bacterie E. coli heeft ongeveer 4600 genen, de mens ergens tussen de 25.000 en 30.000 en er zijn planten bekend met nog veel meer genen. “Het is geen onverwachte publicatie, maar wel een bijzondere”, reageert Bert Poolman, hoogleraar Biochemie aan de Rijksuniversiteit Groningen en directeur van het Center for Synthetic Biology. “Ik was er eerst niet zeker van of je zonder problemen stukken uit een genoom kunt knippen, de nieuwe delen weer aan elkaar kunt plakken en dat het dan ook weer werkt. Maar het is ze toch gelukt om zo een behoorlijk werkende bacterie te maken.”
Van de 473 genen die JCVI-syn3.0 nodig heeft om te leven, te delen en te groeien is van 149 genen de functie niet bekend. Tijdens de persconferentie vertelden de onderzoekers dat dit aantal hoger was dan verwacht. Een lesje in nederigheid, aldus Venter zelf. “Het laat zien hoe complex leven is in zelfs een van de meest simpele vormen. Als we daarvan al een derde van de basale biologische kennis missen, dan hebben we nog een lange weg te gaan.”
Lastig meten
Bert Poolman is wat minder verrast over die ruim 30% onbekende genen. “Als je me vooraf had gevraagd, had ik waarschijnlijk een iets lager percentage genoemd, maar ook van een veel bestudeerde bacterie als E.coli weten we van tien tot twintig procent van de genen niet wat ze doen.”
Hij heeft wel een idee wat die onbekende functies kunnen zijn. “Vaak zijn dat genen die coderen voor een activiteit die je niet eenvoudig kunt meten. Het zijn veelal geen eiwitten met een katalytische activiteit. En dat maakt het lastig om te bepalen wat ze precies doen. Een cel heeft niet altijd alles nodig en sommige eiwitten fungeren dan als een soort parkeerplaats voor andere onderdelen. Maar zo’n functie is heel lastig te meten. Ook zijn er allerlei eiwitten betrokken bij de structuur van de cel. Die eiwitten zijn noodzakelijk om te overleven, maar ze katalyseren geen reacties. Dat maakt het moeilijk om ze bestuderen.”
JCVI-syn3.0 heeft nog steeds alle genen die nodig zijn voor het aflezen van de genetische informatie en het produceren van de eiwitten waarvoor ze coderen. Ook is alles aanwezig wat een cel nodig heeft om de genetische informatie door te geven aan nakomelingen. Maar over hoe ‘minimaal’ dit genoom is, valt nog wel wat te zeggen. De onderzoekers hebben ook genen behouden die zorgen voor een acceptabel groeitempo. En JCVI-syn3.0 leeft in een medium dat heel rijk is aan voedingsstoffen en alle bouwstenen bevat die de bacterie nodig heeft. Genen voor de biosynthese van bijvoorbeeld aminozuren, de bouwstenen van eiwitten, heeft JCVI-syn3.0 niet nodig. Maar in een minder rijke omgeving zou zo’n bacterie niet overleven.
Eerste leven
Als de omgeving bepaalt hoe minimaal een genoom kan zijn, is het dan wel zinvol om te spreken van ‘het minimale genoom’? Venter is daar helder over. “We noemen het nadrukkelijk een minimaal genoom, niet het. Wat de minimale eisen aan een genoom zijn, zal variëren per omgeving waarin dat organisme leeft.”
Maar als de omgeving zoveel invloed heeft, is het dan aannemelijk dat er op verschillende plekken onafhankelijk van elkaar leven is ontstaan dat paste bij die specifieke omgeving? Aan Poolman de vraag wat dat betekent voor het ontstaan van het eerste leven.
“Dat is een lastige vraag. Voor een cel zijn er twee mogelijkheden om aan essentiële bouwstenen zoals aminozuren en vitaminen te komen. Je haalt ze uit de omgeving of je maakt ze zelf. We kennen bacteriën die in staat zijn om uit alleen koolstofdioxide, waterstof en wat ammoniak een relatief complex molecuul als een aminozuur te maken. Maar dat vraagt wel een ingewikkelde cellulaire machinerie en het lijkt me niet waarschijnlijk dat de allereerste cellen daar meteen over beschikten. We weten dat aminozuren ook chemisch zijn ontstaan, zonder biosynthese. De kans is daarom groter dat het eerste leven is ontstaan in een omgeving met een hoge concentratie aan noodzakelijke moleculen, waardoor een primitieve cel niet alles zelf hoefde te maken. Het vermogen om dat wel te kunnen is gedurende de evolutie ontwikkeld. Bovendien leven de Mycoplasma-bacteriën, waar deze synthetische bacterie een afgeleide van is, van nature in heel grondstofrijke omgevingen. De meeste organismen zullen maximaal gebruik maken van wat hun omgeving te bieden heeft.”