Levende cellen verbruiken continu energie die ze ook zelf opwekken. Om kunstmatige cellen meer levensecht te maken, is zo’n energievoorziening een voorwaarde. Groningse chemici komen nu met een werkende, moleculaire energiecentrale.
Misschien wel de belangrijkste taak van de levende cellen waar wij (en alles wat leeft) uit bestaan is het opwekken van bruikbare energie. Zonder een continue productie van energie is een levende cel ten dode opgeschreven. Vrijwel iedere cel beschikt daarom over een eigen, behoorlijk ingewikkelde energiecentrale. De onderzoeksgroep van Bert Poolman, hoogleraar biochemie aan de Rijksuniversiteit Groningen, is erin geslaagd om een sterk vereenvoudigde versie van die natuurlijke energiecentrale te bouwen en te laten draaien in kunstmatige cellen.
De centrale van Poolman en collega’s werkt met vier verschillende enzymen; natuurlijke katalysatoren die een chemische reactie versnellen, maar zelf niet veranderen. Samen zorgen de enzymen voor de omzetting van arginine naar het eindproduct ornithine, beide zijn stoffen die van nature voorkomen in cellen. Bij deze omzetting komt voldoende energie vrij om tegelijkertijd ook een molecuul ATP (zie kader) te maken en dat is waar het uiteindelijk om draait. ATP fungeert namelijk als de belangrijkste energiedrager in levende cellen. Het is de oplaadbare batterij waar het leven op werkt.
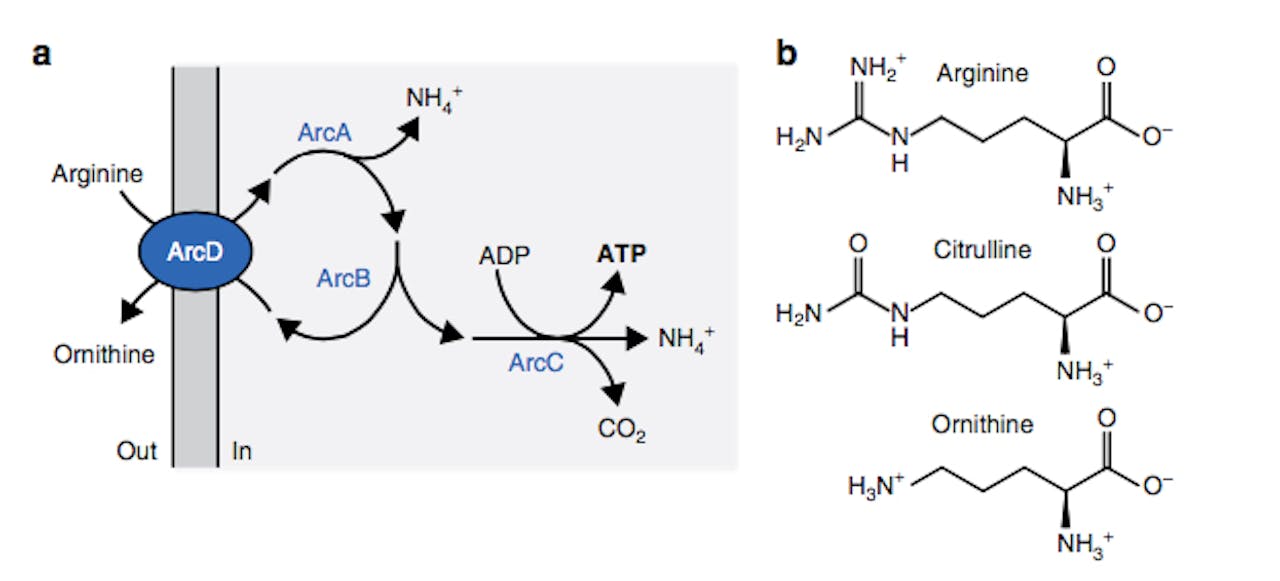
De vier stappen in moleculaire energiecentrale. Stap 1: Het enzym ArcD zit in de membraan van de kunstmatige cel en laat arginine naar binnen. Stap 2: Arginine wordt door ArcA omgezet in citrulline. Stap 3: Het enzym ArcB zet citrulline om in ornithine, waarbij ook meteen stap 4 plaatsvindt: de vorming van ATP uit ADP door het enzym ArcC.
Nature Comm (2019), doi:10.1038/s41467-019-12287-2Synthetische cel
De Groningse moleculaire energiecentrale bestaat volledig uit componenten die van nature in levende cellen, ook de onze, voorkomen. Bovendien werkt de centrale volgens dezelfde principes als het biologische voorbeeld en is het eindproduct ook gelijk, namelijk ATP. Je kunt je afvragen waarom een onderzoeker al die moeite doet. Het vergt namelijk flink wat tijd en inspanning voordat de boel echt draait en de centrale het, zoals nu, een aantal uren volhoudt. “Dit onderzoek is onderdeel van een veel groter project”, legt Poolman uit, “namelijk het bouwen van een synthetische levende cel.” Binnen dit zogeheten BaSyC-programma is Poolman met zijn groep verantwoordelijk voor de energievoorziening van de synthetische cel.
“Ons overkoepelende doel is om vanuit bestaande biologische bouwstenen en componenten een levende cel te reconstrueren, opnieuw in elkaar te zetten en vervolgens nieuwe functies toe te voegen. Een levende cel zit zo razend ingewikkeld in elkaar, dat we eerst proberen om een sterk vereenvoudigde versie te maken. Alleen al bij de productie ATP zijn in het menselijk lichaam ongeveer honderd verschillende eiwitten en enzymen betrokken. Daarom zijn we op zoek naar de meest simpele manieren om een cel na te bouwen. Dus maken we gebruik van systemen die dezelfde functie vervullen, zoals het genereren van energie, maar die veel eenvoudiger in elkaar zitten.”
De centrale werkt al in een celachtige omgeving. Die ‘cellen’ zijn holle bolletjes met een omhulsel van vettige moleculen, net zoals een levende cel ook een membraan van vettige moleculen heeft. Het opbouwen van de energiecentrale is volgens Poolman nogal een ‘houtje-touwtjeproces’, dat door veel proberen is uitgevogeld. “Zolang we niet meer dan tien à twintig componenten gebruiken, lukt het zo nog wel. Maar voor de uiteindelijke synthetische cel met honderden componenten moeten we gebruikmaken van zelfassemblage, waarbij systemen zichzelf in elkaar zetten. Levende cellen hebben ook een complete machinerie om zichzelf op te bouwen.”
Verzuring
Op basis van één molecuul arginine kan de kunstmatige cel één molecuul ATP produceren. Een heel efficiënt proces, aldus Poolman. Maar dat vereist wel dat er ook continu ATP wordt verbruikt. Gebeurt dat niet, dan valt het systeem stil. De omzetting van arginine naar ornithine verloopt namelijk niet rechtstreeks, maar via een tussenproduct, citrulline. Dat wordt omgezet in ornithine, maar alleen als er tegelijkertijd ook een molecuul ADP wordt omgezet in ATP. Er moet dus wel voldoende ADP aanwezig zijn en dat is alleen het geval als het gevormde ATP weer snel wordt verbruikt.
Is de ATP-consumptie te laag, dan wordt de concentratie citrulline zo hoog dat de enzymen in de membraan het naar buiten gaan pompen. Dan heb je dus per uitgepompte citrulline een molecuul arginine verspild. Bovendien hopen ook andere bijproducten zich op en dat leidt tot verzuring. Poolman wijst erop dat deze verzuring geen typisch probleem van zijn kunstmatige cel is. “Dit zien we in levende cellen ook gebeuren. Denk maar aan glucose, een belangrijke brandstof voor ons lichaam. Als dat niet compleet wordt omgezet, krijg je de vorming van melkzuur. De bekende verzuring van je spieren.”
Niet perfect
Om de ATP-consumptie op peil te houden, is een tweede systeem aan de ‘cellen’ toegevoegd met ook een enzym in de membraan. Dat treedt in werking als de ion-sterkte stijgt; in dit geval de concentratie van de positief geladen ionen die onder meer voor de verzuring zorgen. Het enzym pompt een ander molecuul naar binnen, waardoor het volume stijgt en de ion-sterkte weer daalt. Voor dit pompen gebruikt het enzym ATP en zo zorgt de koppeling van beide systemen voor een goede balans in vraag en aanbod van ATP.
Het is volgens Poolman een bekende misvatting om het natuurlijke voorbeeld als perfect te zien. “Als je goed naar een levende cel kijkt dan is het ronduit opmerkelijk dat het allemaal werkt, want alles is imperfect.” De mate van imperfectie wordt de laatste jaren steeds duidelijker, zegt hij. “We hebben allemaal geleerd dat enzymen ontzettend specifiek zijn, maar nu we veel gevoeligere meettechnieken hebben blijkt dat ze veel meer stoffen omzetten dan we dachten. Zo specifiek zijn ze helemaal niet. Inmiddels wordt er al gesproken van ‘underground biochemistry’, een soort verborgen chemie van de levende cel die langzaam aan het licht komt.”
De groep van Poolman is inmiddels druk bezig om de energievoorziening verder uit te breiden en direct te koppelen aan nuttige functies. “We zijn onder meer bezig om de ATP-productie meteen te gebruiken om onze ‘cellen’ zelf de vettige bouwstenen van de membraan te laten maken. Dat is een eerste stap om ook een kunstmatige cel te laten groeien.”

