Cholesterol kun je goed gebruiken als bouwsteen. Het vormt van nature nanodeeltjes om ladingen te vervoeren. Chemicus Willem Mulder wil die deeltjes gebruiken om het afweersysteem te stimuleren of juist te remmen. Hij kreeg onlangs een Vici-subsidie van € 1,5 miljoen voor dat idee.

Willem Mulder studeerde scheikunde aan de Universiteit Utrecht en promoveerde in 2006 aan de Technische Universiteit Eindhoven. In datzelfde jaar vertrok hij naar het Mount Sinaï ziekenhuis in New York, waar hij het nanogeneeskundelab oprichtte. Sinds 2013 is hij ook hoogleraar aan het AMC Amsterdam. Zijn onderzoek richt zich op nanodeeltjes voor diagnostiek en therapie, vooral voor hart- en vaatziekten en ziekten die te maken hebben met het immuunsysteem.
Willem Mulder, met toestemmingHet verpakken van geneesmiddelen in nanodeeltjes – piepkleine ‘capsules’ van enkele tientallen tot honderden nanometers groot – staat sterk in de belangstelling. Dit moet zorgen voor meer effectiviteit en minder bijwerkingen, omdat de nanodeeltjes het geneesmiddel precies op de juiste plek in het lichaam afgeven.
Willem Mulder houdt zich ook bezig met het ontwikkelen van geschikte nanodeeltjes. Hij is directeur van het nanogeneeskundelab van het Mount Sinaï medisch centrum in New York en hoogleraar cardiovasculaire nanogeneeskunde aan het AMC in Amsterdam. Voor inspiratie kun je het best naar de natuur kijken, vindt Mulder. “Ons lichaam bevat een prachtig materiaal dat we heel goed kunnen gebruiken, namelijk HDL, beter bekend als het goede cholesterol.”
Ploegendiensten
Een belangrijk eiwit uit HDL is apoA-1. “Dat wordt gemaakt in de lever en gaat vanaf daar via de bloedbaan op reis door het lichaam om overal vetten op te pikken”, legt Mulder uit. Meerdere apoA-1-eiwitten en fosfolipiden — de bouwstenen van celmembranen — vormen samen een nanodeeltje. Dit deeltje neemt vetmoleculen op en belandt uiteindelijk in de darmen, waar het opgeslagen vet via de stofwisseling wordt verwerkt.
De nanodeeltjes herkennen eerst specifieke cellen van het immuunsysteem en nemen dan de vetten op. “Deze selectieve transportfunctie kunnen we mooi gebruiken om lichaamseigen nanodeeltjes te maken, waarmee je ook andere ladingen dan vetten kunt vervoeren.” Dat ‘lichaamseigen’ kun je letterlijk nemen. Mulder: “We halen HDL uit menselijk plasma dat we van de bloedbank krijgen. Dat is veel werk overigens: als we weer een nieuwe voorraad nodig hebben draaien we ploegendiensten in het lab. Dan gaan er echt liters en liters plasma doorheen.”
&feature=youtu.be
Geavanceerde Lego
Mulder en zijn groep gebruiken vervolgens het eiwit apoA-1 als bouwsteen. “ApoA-1 vormt uit zichzelf een gedraaide structuur zoals een kurkentrekker met een waterminnende en een watermijdende kant. Samen met fosfolipiden vormt het nog weer grotere en heel bijzondere structuren. Je kunt deze moleculen zien als een soort geavanceerde Lego, waarmee je echt heel leuke dingen kunt bouwen.”
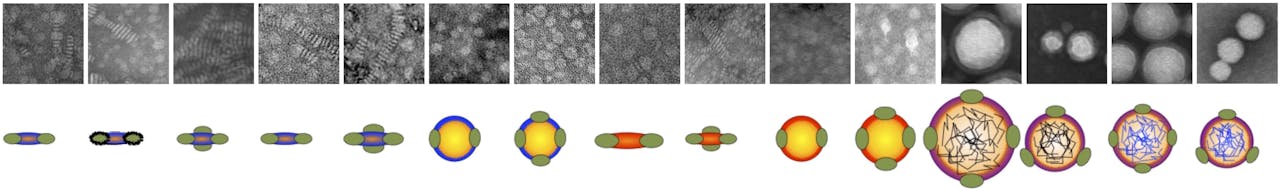
Boven: microscopische opnamen van verschillende nanodeeltjes op basis van HDL en fosfolipiden. Onder: schematische weergaven van de doorsnede van die deeltjes. Het eiwit apoA-1 is aangegeven in het groen.
J. Tang, et al, PNAS (2016), doi:10.1073/pnas.1609629113Dat heeft inmiddels geleid tot een flinke collectie nanobiologics, zoals Mulder de lichaamseigen nanodeeltjes noemt. Die kun je gebruiken voor het afgeven van geneesmiddelen in het lichaam, maar er zijn nog veel meer mogelijkheden. Mulder heeft onlangs een zogeheten Vici-subsidie van € 1,5 miljoen gekregen voor een spannend idee, namelijk om met nanobiologics ons afweersysteem te ‘trainen’. Een plan geïnspireerd door de ontdekking van de Nijmeegse hoogleraar Mihai Netea dat ook ons aangeboren, aspecifieke immuunsysteem een geheugen heeft.
Vliegende start
Mulder: “Als een immuuncel in contact komt met een ziekmakende bacterie of andere bedreiging, dan wordt die immuuncel geactiveerd. Netea heeft ontdekt dat die activatie een tijdje kan blijven hangen. Als er binnen een bepaalde tijd opnieuw contact is met een lichaamsvreemde stof, dan reageert het immuunsysteem extra heftig. Alsof de afweerreactie een vliegende start maakt.”
Het plan van Mulder is om dit vermogen van het immuunsysteem te gebruiken om de respons te versterken of te onderdrukken. Bij het immuunsysteem draait namelijk alles om de balans tussen afweren en tolereren. “In patiënten met kanker wil je een heftige afweerreactie tegen de tumor, terwijl je in patiënten die een transplantatie ondergaan juist geen reactie tegen het nieuwe orgaan wil. Wij denken dat we met onze nanobiologics een manier hebben om de kracht waarmee het aangeboren immuunsysteem reageert, te reguleren.”
Bij muizen hebben Mulder en collega’s al laten zien dat je een extra sterke respons kunt opwekken. “We hebben het immuunsysteem van de muizen getraind door ze te behandelen met nanobiologics gevuld met een lichaamsvreemde stof. Hierdoor raken de immuuncellen geactiveerd, ze gaan als het ware in de startblokken staan. Als we die cellen vervolgens blootstellen aan een heel andere lichaamsvreemde stof, reageren ze heel heftig. Veel sterker dan normaal. Dit principe kun je wellicht gebruiken om de afweerreactie tegen tumoren flink te versterken.”
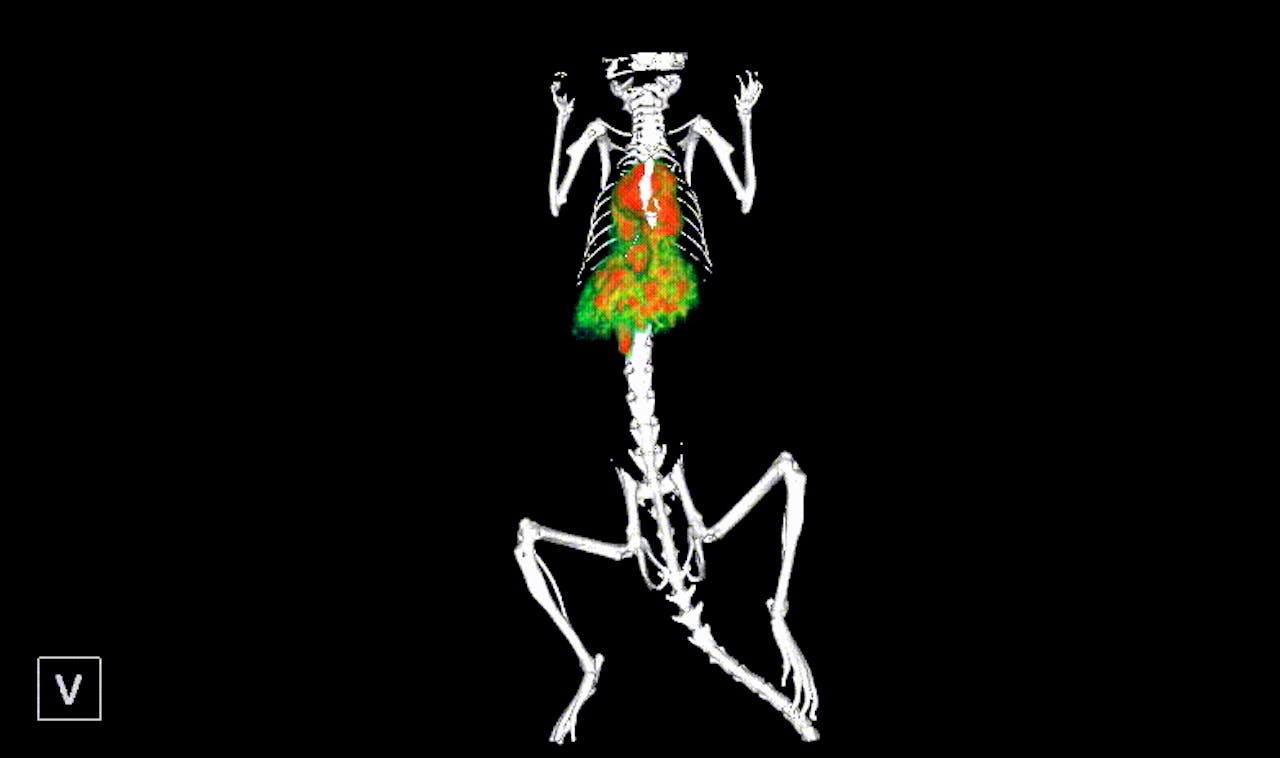
Distributie van nanobiologics in een muis. De nanodeeltjes hopen zich vooral op in de lever en de milt.
W.J.M. Mulder, met toestemming aan NEMO KennislinkMinder troep
De andere mogelijkheid is het onderdrukken van de afweer. Deze aanpak is al verder gevorderd. “We hebben in muizen laten zien dat je de afstoting van een getransplanteerd orgaan helemaal kunt voorkomen. We hebben de muizen in een tijdsbestek van vijf dagen driemaal een dosis nanobiologics gegeven, met daarin een stof die een bepaald biologisch proces in immuuncellen blokkeert. Het resultaat is dat de balans in het immuunsysteem verandert en dat het ‘tolerant’ is ten opzichte van het getransplanteerde orgaan.”
De behandeling had een enorm effect. “Na honderd dagen was het nieuwe orgaan nog steeds niet afgestoten. In muizen mag je dan spreken van tolerantie. En dat met maar drie behandelingen, terwijl je normaal gesproken dagelijks immuun-onderdrukkende middelen moet toedienen.”
Of je deze aanpak ook naar mensen kunt vertalen kan Mulder nu nog niet zeggen. “Dat is echt koffiedik kijken; wat wij doen is sleutelen aan de basis. Maar ik vind deze studie veelbelovend. Patiënten die nu een transplantatie ondergaan moeten een enorme hoeveelheid troep slikken om afstoting te onderdrukken. Met als serieus risico dat ze van iets anders heel ziek worden. Ons idee is dat je niet meer het complete immuunsysteem platlegt. Je maakt patiënten daardoor veel minder vatbaar voor infecties. Of het allemaal gaat werken moeten we nog zien, maar als het lukt zal deze methode veel subtieler werken dan hoe we het nu doen.”

