Kapotte organen repareren, dat is de grote uitdaging binnen de regeneratieve geneeskunde. En dat was ook de uitdaging waarmee hoogleraar Christine Mummery begon aan haar onderzoek naar het hart. Maar reparatie van het hart met stamcellen bleek moeilijker dan gedacht. En dus gooide Mummery het over een andere boeg.
Hoogleraar Christine Mummery begon haar onderzoek naar hartreparatie in 2003 met een simpel idee: gezonde hartcellen maken uit stamcellen en deze direct inspuiten in de hartspier. Het doel was hartfalen voorkomen, bij patiënten die bijvoorbeeld net een hartinfarct hebben gehad en waarbij een deel van de hartspier niet meer werkt.
Tegenvaller
Dat eerste idee blijkt al snel moeilijk uitvoerbaar. Mummery: “Er was geen geschikt proefdier voorhanden. De muis is geen goed model voor hartziekten. Het muizenhart klopt ruim vijfhonderd keer per minuut, dat van de mens maar zestig keer. Bovendien gaat de hartslag van een muis niet omhoog bij stress en die van de mens wel. Het hart van een varken is een beter model, maar daarbij is het weer heel lastig om de afweer te onderdrukken, waardoor stamcellen snel worden afgestoten.”
Naast dit probleem van een goed proefdiermodel dook ook een praktisch probleem op. Het hart is één bonk spier. Hoe ga je gezonde hartcellen daar tussen krijgen? De stamcellen komen niet zomaar overal. “Ik vergelijk het altijd met een kauwgombal”, vertelt Mummery. “Als je daar een rode kleurstof in spuit, wordt niet de hele kauwgombal rood, maar slechts een klein stukje. En dat werkt bij het hart net zo. Het inspuiten van losse cellen in de hartspier is dus geen succes. Een tegenvaller, maar dat hoort ook bij onderzoek doen. En we hebben door de experimenten wel veel geleerd over het menselijk hart.”
Acht verschillende hartcellen
In 2009 begon Mummery met frisse moed en een nieuwe doelstelling: het maken van een synthetisch stukje hart. Om een synthetisch hart te kunnen maken, moet je eerst alle celtypen van het hart in het laboratorium kunnen namaken. Dat klinkt makkelijk, maar het is een enorme uitdaging. Een foetaal hart bestaat voor zestig procent uit kloppende hartcellen, maar bij een volwassen hart is dat nog maar dertig procent. Binnen de kloppende hartcellen heb je ook nog verschillende typen. De cellen van de boezems zien er bijvoorbeeld net iets anders uit dan de cellen van de hartkamers. Daarnaast zitten er in het hart nog bloedvatcellen die het hart zelf van zuurstof voorzien, bindweefselcellen, die zorgen voor stevigheid, en pacemakercellen, die het hartritme regelen.
“Je weet hoe een embryo hartcellen maakt, maar ontrafelen welke signalen daarvoor nodig zijn, is nog een hele klus”, legt Mummery uit. “Embryo’s van de zebravis en de muis komen hierbij goed van pas. Je kunt bij die dieren steeds één ‘signaal’ uitzetten en kijken wat er gebeurt met de ontwikkeling van het hart. Als je dat doet en je ziet, bijvoorbeeld, dat er geen pacemakercellen worden gemaakt, dan kun je dat uitgeschakelde signaal gaan toevoegen aan stamcellen in de hoop dat zij juist wel pacemakercellen gaan maken.” Via deze aanpak is het uiteindelijk gelukt om acht verschillende hartceltypen te maken.
Hartcellen testen
Samen met engineers ging Mummery op zoek naar de perfecte matrix voor de gekweekte hartcellen. “In het lichaam groeien hartcellen op een zacht substraat. Dat is een goede omgeving voor de cellen, dus dat hebben we in het laboratorium ook nodig. We laten de cellen groeien op een synthetisch polymeer, een beetje vergelijkbaar met silicone. Dat polymeer plaatsen we dan op een chip met spiraalvormige elektroden erin en een vacuüm eronder. De spiraalvormige elektroden vormen een soort reksysteem dat de cellen in beweging brengt. Door het vacuüm te veranderen, kun je de hartslag aanpassen. Zo kunnen we zieke hartcellen testen in rust, maar bijvoorbeeld ook bekijken wat er gebeurt als een patiënt gaat sporten”, vertelt ze.

Gekweekte hartcellen worden getest op een flexibele chip. De chips zijn op dit moment nog te groot om in standaard kweekbakjes te brengen. In samenwerking met de TU Delft probeert Mummery het systeem nu te verkleinen. Als dat lukt, kunnen de gekweekte hartcellen op grote schaal gebruikt worden. Bijvoorbeeld voor medicijnonderzoek.
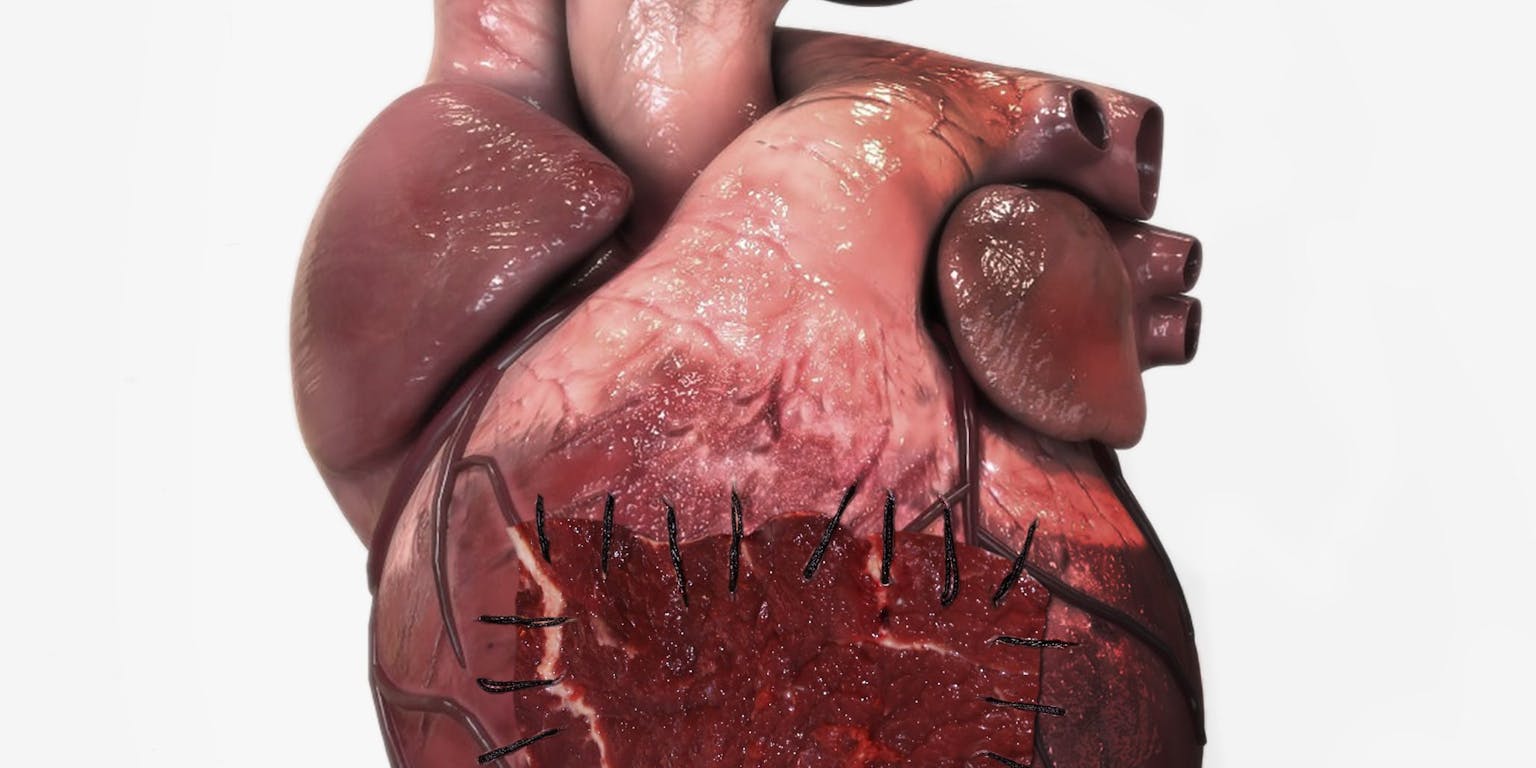
Berend van der Meer (LUMC)Het systeem van Mummery fungeert nu nog voornamelijk als testmodel, maar in de toekomst ziet zij wel toepassingen voor de patiënt. “We zouden een stukje synthetisch hart kunnen gebruiken als patch of pleister op een beschadigd hart. Ook daar zullen haken en ogen aanzitten. Na een hartinfarct zit schade vaak door het hele hart, maar zo’n pleister plak je aan de buitenkant. Heeft dat zin of moet je de pleister op een andere plek aanbrengen? Bijvoorbeeld net onder de buitenste laag van het hart. Dat zal vergelijkbaar zijn met iets onder de schil van een sinaasappel brengen, zonder de sinaasappel verder te schillen. Repareren van het hart is niet makkelijk, maar dat betekent niet dat je het niet moet proberen.”