In het recente verleden is er veel ophef geweest over stier Herman, het eerste dier met een ‘menselijk’ gen, en over het gekloonde schaap Dolly. Tegenwoordig concentreert de aversie tegen gentech zich op neveneffecten, zoals de vermeende kwade bedoelingen van zadengigant Monsanto. Actievoerders opgelet: er is nu iets veel ingrijpenders aan de hand. De genetische kettingreactie komt eraan.
Je kon er op wachten, en het wachten duurde niet lang: in november 2015 beschreven Amerikaanse onderzoekers in het vakblad PNAS hoe ze malariamuggen zodanig genetisch veranderd hadden, dat in principe één exemplaar de complete populatie malariamuggen in een regio in een paar jaar tijd resistent kan maken tegen de malariaparasiet. Omdat malaria niet van mens op mens overdraagbaar is, zou dit betekenen dat malaria in die streek voorgoed is uitgeroeid.
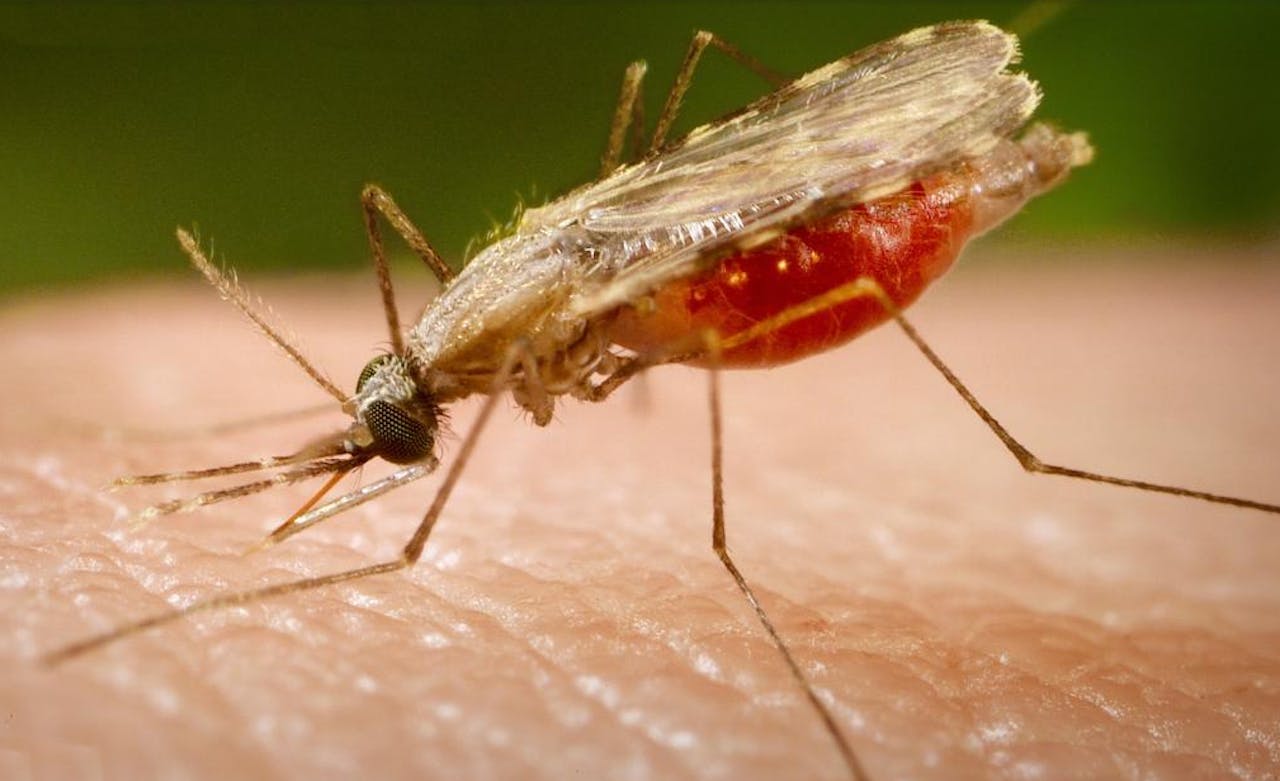
Een malariamug die bloed zuigt bij een mens. Als de mug besmet is met de malariaparasiet Plasmodium falciparum, brengt hij die op dit moment over op de mens, die dan malaria krijgt.
wikimediaDe revolutionaire gentechnologie die dit mogelijk maakt, was in maart 2015 in vakblad Science al beschreven door twee van hen, Valentino Gantz en Ethan Bier. Het betreft de Mutagenic Chain Reaction, de genetische kettingreactie, gebaseerd op een ook pas in 2013 ontwikkelde gentechniek, Crispr/Cas9. Datzelfde Science riep Crispr/Cas9 onlangs uit tot dé wetenschappelijke doorbraak van 2015.
Telescoopvizier
Het ziet ernaar uit, dat deze nieuwe gentechniek in een adembenemend tempo bezig is zijn beloften waar te maken. Technieken om aan genen te sleutelen bestaan natuurlijk al langer, en worden ook veel gebruikt bij planten en bacteriën. Maar die oude gentechniek is inefficiënt en ongericht. Ingebrachte genen komen niet, of op willekeurige plekken, in het genoom terecht en werken vaak niet. Met Crispr/Cas9 kun je heel gericht – en in sommige gevallen met bijna honderd procent succes – een gen op exact de juiste plaats in het DNA van cellen zetten. Dat kunnen lichaamscellen zijn, maar ook zaad- of eicellen, zodat de verandering meteen erfelijk overdraagbaar is.
De oude gentechnieken laten zich vergelijken met een hagelgeweer waarmee je geblinddoekt op het genoom schiet, terwijl Crispr/Cas9 een geweer met telescoopvizier is. De eerste experimenten met Crispr/Cas9 op menselijke embryo’s zijn al gedaan, zoals bleek in april 2015. Dat veroorzaakte toen grote bezorgdheid onder onderzoekers in dit vakgebied.
De Mutagenic Chain Reaction (MCR) doet hier nog een flinke schep bovenop, wat vreemd genoeg nog weinig aandacht gekregen heeft buiten de kring van onderzoekers die hier aan werken. Het blijkt namelijk mogelijk, om een met Crispr/Cas9 ingebracht gen te voorzien van een soort breekijzer waarmee het de gewone overerving buitenspel zet.
Een gewone lichaamscel heeft voor elke eigenschap twee genen in zijn DNA zitten, omdat zijn chromosomen in tweevoud voorkomen. Bij gewone genetische modificatie wordt slechts één van beide kopieën vervangen door het aangepaste gen. Maar bij de genetische kettingreactie zorgt het breekijzer ervoor, dat dit MCR-gen zich automatisch kopieert naar het partnerchromosoom en het normale gen eruit snijdt.
‘Besmettelijk’ gen
Het komt er op neer dat een organisme met zo’n MCR-gen, ook als het met een niet-gemodificeerde soortgenoot paart, alleen maar kinderen krijgt die ook twee exemplaren van dit gen hebben. En die leveren op hun beurt weer kleinkinderen met ook allemaal twee exemplaren van dit gen. Het MCR-gen verspreidt zich dus als een virus door de populatie, zij het dat paring voor ‘besmetting’ van alle nakomelingen zorgt. Deze genetische kettingreactie is een dramatisch contrast met normale overerving van een gemodificeerd gen, dat in een natuurlijke populatie steeds verder ‘verdund’ zou raken en niet of nauwelijks voet aan de grond zou krijgen.
Dat is heel handig als je met een paar in het laboratorium gemodificeerde muggen een populatie van miljarden muggen resistent wilt maken tegen de malariaparasiet. Maar zelfs de onderzoekers die dit kunststukje voor elkaar kregen, schrijven in hun artikel in PNAS: “We zijn ons heel goed bewust van de aanzienlijke risico’s die met deze zeer invasieve techniek gepaard gaan, want als er geen strenge voorzorgsmaatregelen genomen worden, kunnen MCR-organismen onbedoeld in het milieu terechtkomen. We zijn het daarom eens met degenen die zeggen dat een dialoog over dit onderwerp met de hoogste urgentie gevoerd moet worden.”
Exponentiële verspreiding
In de begintijd van de gentechnologie was dat de grote angst van de tegenstanders: stel dat er een genetisch gemodificeerde muis ontsnapt die zich in het wild gaat voortplanten? Die angst was toen grotendeels onzinnig, juist omdat de gemodificeerde genen normaal overerfden. Slechts als de gemodificeerde muizen een duidelijk voordeel hebben in de strijd om het bestaan, zouden ze op den duur – door natuurlijke selectie – een groter aandeel in de populatie krijgen.
Maar MCR-genen verspreiden zich exponentieel en kunnen in tien of twintig generaties een populatie helemaal overnemen. Voor muggen duurt dat twee regenseizoenen, voor muizen een paar jaar. Het idee, dat je met één of enkele gemodificeerde organismen een niet meer te stoppen genetische kettingreactie in gang kunt zetten die de hele wereld over kan gaan, is zowel fascinerend als angstaanjagend.
Gek genoeg merken we heel weinig (niets eigenlijk) van de dialoog waartoe onder meer Gantz en Bier oproepen. Er staan geen actievoerders voor de desbetreffende laboratoria, Greenpeace maakt zich over gentech alleen nog druk als Monsanto erbij betrokken is. Blijkbaar is het grote publiek gewend geraakt aan gentech; het is weliswaar iets van foute multinationals en op de een of andere, vage manier niet milieuvriendelijk, maar in deze tijd nou ook weer niet iets om je over op te winden. Terwijl daar nu meer reden toe is dan ooit tevoren.
In de filmklassieker ‘The boys from Brazil’ uit 1978 zien we hoe door klonen tientallen replica’s van Adolf Hitler op de wereld gezet worden. Het schrikbeeld van een tiran die zijn kwalijke eigenschappen over de hele mensheid probeert te verspreiden krijgt er door de genetische kettingreactie nog een dimensie bij. Iemand die narcistisch en machtig genoeg is, zou bepaalde genvarianten van zichzelf met Crispr/Cas9 en de genetische kettingreactie in een aantal (desgewenst door hemzelf) bevruchte eicellen kunnen laten plaatsen.
De mensen die daaruit opgroeien, zijn geen klonen van de tiran, maar ze zouden bepaalde eigenschappen, zoals agressiviteit of superioriteitsgevoel aan al hun kinderen doorgeven, en die weer aan al hun kleinkinderen, enzovoort, totdat na vele generaties de complete mensheid die genvarianten heeft. Wanneer iemand als de Noord-Koreaanse leider Kim-jong un hier van hoort, zou hij het best eens in zijn hoofd kunnen halen, om sommige van zijn genen in de hele toekomstige Noord-Koreaanse bevolking in te planten. Het gaat er niet eens om, dat het waarschijnlijk onmogelijk is om Kim-jong-unigheid vast te pinnen op een paar genen, maar het is een idee dat zal appelleren aan dictators met grootheidswaanzin. Een mensheid met alleen maar blauwe ogen, dat is nog tot daar aan toe, maar willen wij iemand als Kim Jong-un laten proberen om de rest van de mensheid met zijn favoriete eigenschappen te besmetten?

