Vitaminen zorgen ervoor dat de enzymen in ons lichaam hun werk kunnen doen. Voor de chemische industrie zijn enzymen interessant omdat ze de productieprocessen veel ‘groener’ kunnen maken. Caroline Paul van de TU Delft ontwerpt synthetische vitaminen die grootschalige toepassing van enzymen mogelijk moeten maken.

Op het eerste gezicht lijken de processen in een chemische fabriek niet op wat er in ons lichaam gebeurt. Toch zijn er veel overeenkomsten. In beide gevallen draait het om het maken of verbreken van chemische bindingen. Moleculen dienen te worden opgeknipt of aan elkaar gekoppeld. Er moet een waterstofatoom bij of af. Of misschien wil je een koolstofatoom vervangen door een stikstofatoom. Wat er ook moet gebeuren, de kans is groot dat het niet vanzelf gaat. Vaak is er een katalysator nodig.
Een katalysator is een stof die een chemische reactie sneller laat verlopen, maar zelf niet meereageert. Als de reactie is voltooid, is de katalysator klaar om het hetzelfde kunstje nog eens uit te voeren. “De meeste industriële katalysatoren bevatten metalen, soms heel zeldzame als platinum of palladium. Dat maakt ze duur en niet duurzaam. Bovendien heb je naast de katalysator vaak nog ongezonde, milieubelastende chemicaliën nodig”, vertelt dr. Caroline Paul, postdoc onderzoeker bij de Biokatalyse groep van de Technische Universiteit Delft.

Co-factor
Paul richt haar blik daarom op natuurlijke katalysatoren: de enzymen. Levende cellen beschikken over een heel arsenaal aan verschillende enzymen die stuk voor stuk hun katalytische functies uitvoeren zonder dat ze giftige oplosmiddelen of extreme temperaturen nodig hebben. Een groot verschil met industriële katalysatoren. “We willen daarom de huidige niet-duurzame katalysatoren graag vervangen door enzymen, maar dat gaat niet zomaar. Enzymen hebben namelijk een specifieke hulpstof nodig om hun werk te doen. Deze hulpstof noemen we een co-factor. En het probleem is dat die co-factoren vaak niet stabiel zijn en dat maakt het lastig om enzymen op grote schaal in de industrie te gebruiken.”
De instabiliteit van de co-factoren is voor levende cellen geen probleem, omdat ze daar doorlopend worden gemaakt. Paul: “Er is altijd voldoende co-factor aanwezig. Maar voor industriële toepassingen, die niet in levende cellen plaatsvinden, is dat wel een probleem. Hier moet de co-factor steeds worden toegevoegd en dat drijft de kosten op. We willen daarom dat de co-factor langere tijd werkzaam blijft en niet na een keer reageren uiteenvalt, zodat het gebruik goedkoper wordt.” Haar onderzoek richt zich op het stabieler maken van de co-factor en dat doet ze door synthetische co-factoren te maken die heel sterk lijken op de natuurlijke hulpstof, maar minder snel worden afgebroken.
Geneesmiddelen
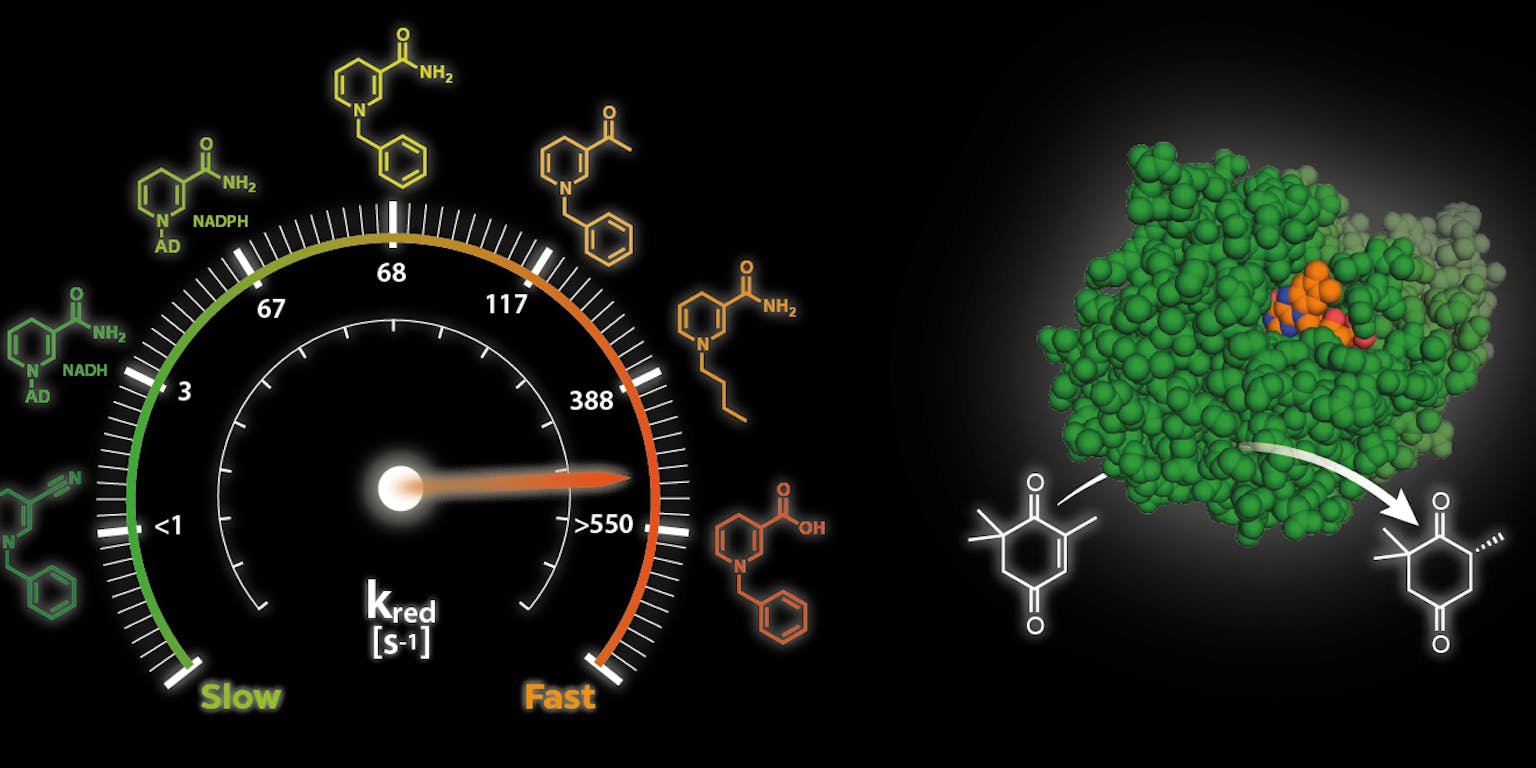
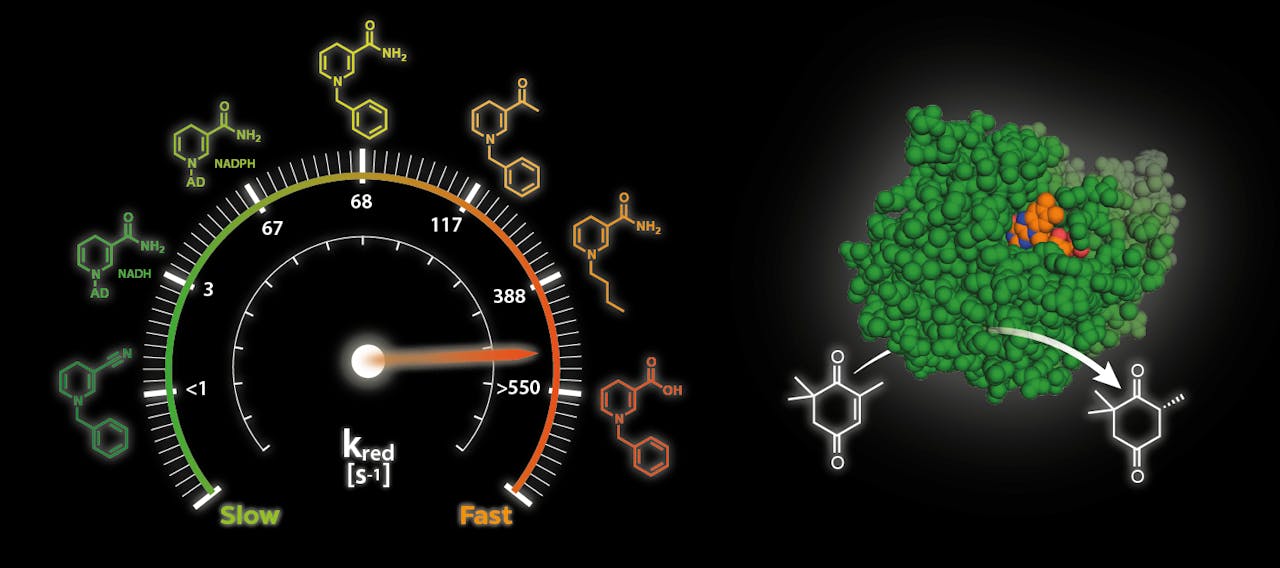
Centraal in het werk van Paul staat de nicotinamide co-factor. Deze speelt een grote rol bij meerdere enzymatische reacties in levende cellen. De nicotinamide co-factor is bijvoorbeeld essentieel voor een goed verloop van citroencyclus, een belangrijk onderdeel van de stofwisseling waarbij suikers, eiwitten en vetten worden omgezet en verwerkt.
Maar Paul denkt dat deze co-factor ook elders nuttig is. “De nicotinamide co-factor zorgt ervoor dat een familie van enzymen genaamd oxidoreductases hun werk doen. Deze enzymen kunnen heel veel verschillende chemische omzettingen katalyseren. Ze zetten bijvoorbeeld dubbele bindingen om in moleculen in een enkele binding. Dat doen ze heel zorgvuldig, waardoor het product steeds precies dezelfde ruimtelijke structuur heeft. Vooral voor moleculen die worden toegepast in geneesmiddelen is dat heel belangrijk, maar ook voor de productie van onder meer aminozuren en vitaminen is die selectiviteit van belang. We denken dat oxidoreductases daar veel beter in zijn dan de huidige industriële katalysatoren. Maar dan moeten we wel zorgen voor een stabielere en goedkopere versie van de nicotinamide co-factor.”
Vergroenen
Cellen maken de nicotinamide co-factor uit vitamine B3. Paul neemt ook vitamine B3 als uitgangspunt om haar biomimics te maken, co-factoren die heel sterk lijken op hun natuurlijke voorbeeld. “Eigenlijk probeer ik betere vitaminen voor de enzymen te maken, zodat ze nog beter gaan presteren.”
Ze is er inmiddels in geslaagd om op heel kleine schaal in het laboratorium, een enzym te laten werken met een synthetische co-factor. Een mooi resultaat, maar ze is er nuchter over. “We staan nog echt aan het begin. Om synthetische co-factoren op grote schaal in te zetten, moeten we precies begrijpen welke kenmerken zo’n nagebootste co-factor moet hebben zodat het enzym ermee kan werken. Veel synthetische co-factoren die we hebben geprobeerd worden gewoon geweigerd door het betreffende enzym.” Paul sluit daarom niet uit dat ze ook aan het enzym zelf iets zal moeten sleutelen.
“Het kan best zo zijn dat we het enzym een beetje moeten veranderen om te zorgen dat de synthetische co-factor beter aansluit, waardoor ze samen optimaal kunnen functioneren.” Dat brengt uiteraard nog meer werk met zich mee, maar daar schrikt ze niet voor terug. “Dit is echt mijn onderwerp en ik vind het heel spannend onderzoek. Dan is het niet erg als er veel werk ligt. Bovendien kan het een mooi resultaat opleveren. Als het lukt om synthetische co-factoren geschikt te maken voor de industrie kan dat de productie van heel veel stoffen enorm ‘vergroenen’. Synthetische co-factoren kunnen uitgroeien tot een heuse game changer voor de chemische industrie.”