De gedetailleerde kennis die we hebben van een klein aantal virussen verhult dat we van het overgrote deel eigenlijk niets of nauwelijks iets weten. Meer genetisch onderzoek is nodig om oorsprong en evolutie van virussen in kaart te brengen.
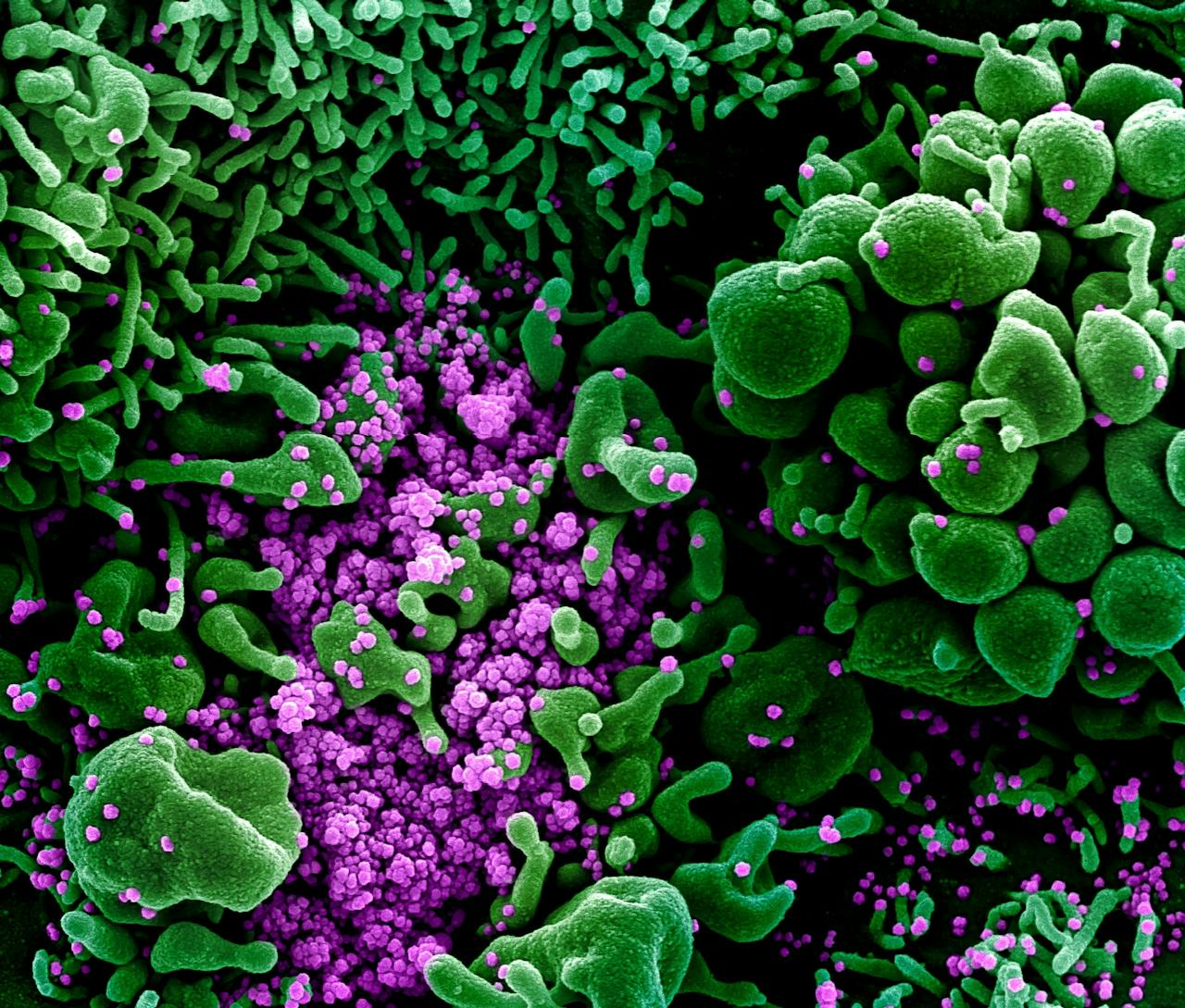
Ingekleurde opname van een stervende cel (groen) die volledig is verwoest door SARS-CoV-2 (paarse bolletjes). Het gebruikte materiaal is afkomstig van een Covid-19-patiënt.
NIAID via Wikimedia Commons CC BY 2.0Bij een nieuwe virusuitbraak volgen de de wetenschappelijke inzichten elkaar snel op. Het virus in kwestie wordt op allerlei manieren onderzocht, met een stroom aan nieuwe kennis tot gevolg. Dat wekt de indruk dat we, ondanks alle onzekerheden, ook al best veel weten van virussen. En voor een deel van de virussen, zeker sommige virussen die mensen en dieren ziek maken, is dat ook zo. Maar het is een heel vertekend beeld. De realiteit is dat we nog extreem weinig weten van de zogeheten virosfeer, de wereld van de virussen. Van het allereerste leven op aarde – en de probeersels die daaraan voorafgingen – weten we al heel weinig, maar over de oorsprong en evolutie van virussen weten we zo mogelijk nog minder.
Een van de redenen zit ‘m meteen al in de formulering van het bovenstaande, waarin een duidelijk onderscheid is tussen ‘leven’ en ‘virussen’. Ondanks dat de discussie over de exacte kenmerken van leven nog volop loopt, is het duidelijk dat virussen enkele van de meest basale eigenschappen missen. Zo hebben virussen geen eigen stofwisseling, wat betekent dat ze niet in hun eigen energiehuishouding kunnen voorzien. Met andere woorden: ze kunnen zichzelf niet draaiende houden, iets wat levende cellen – ook zeer eenvoudige – wel kunnen. Ook kunnen virussen zich, in tegenstelling tot ‘echte’ levensvormen, niet zelfstandig voortplanten. Dat lukt alleen als ze een levende cel voor hun karretje spannen. Conclusie: een virus leeft niet.
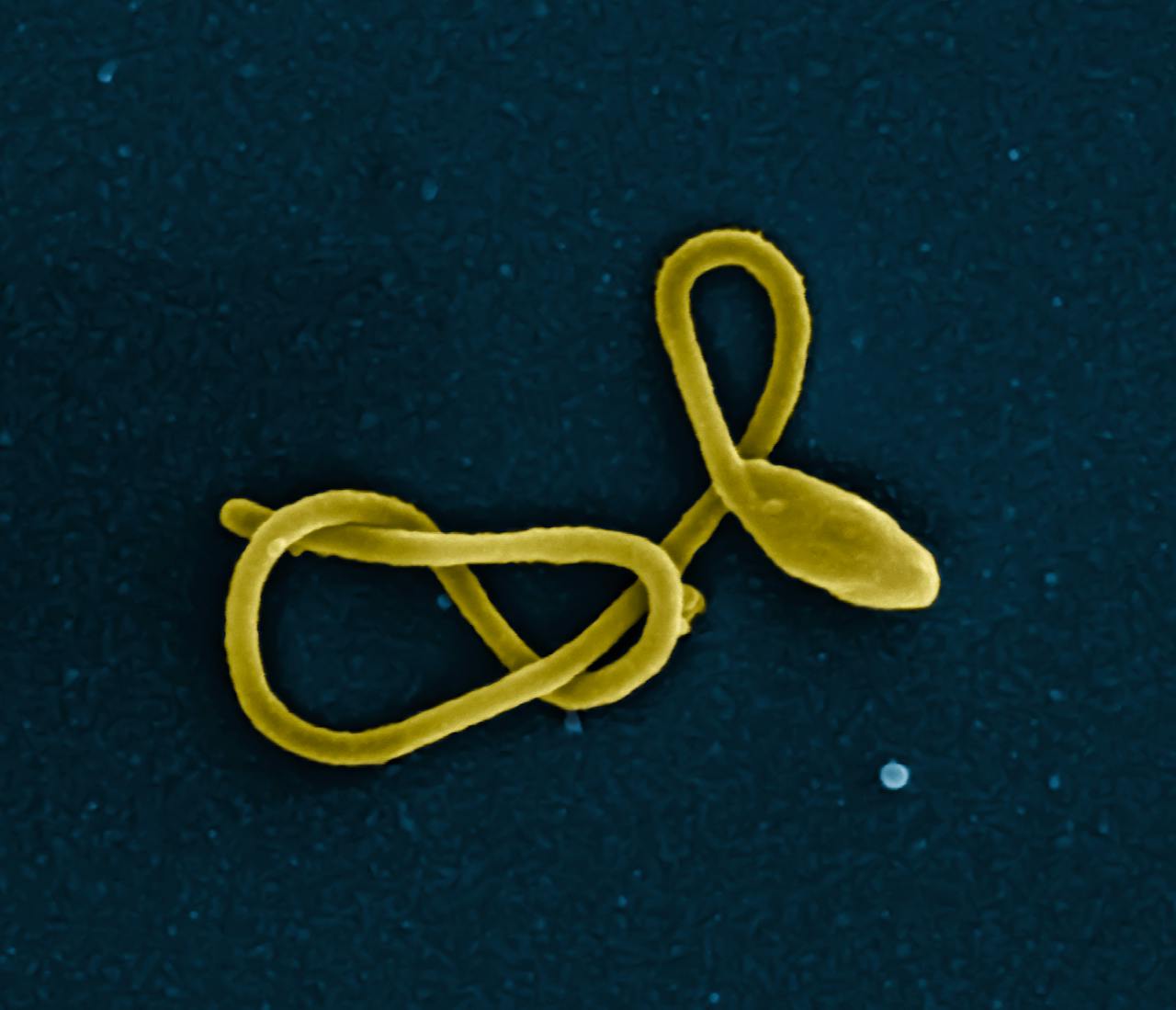
Een enkel ebolavirus, meteen herkenbaar aan de bijzondere vorm.
NIAID via Wikimedia Commons CC BY 2.0Maar daar staat tegenover dat virussen op andere aspecten wel degelijk voldoen aan de eisen van de levende wereld. Zo hebben ze namelijk hun eigen genetisch (erfelijk) materiaal dat de instructies voor hun bouw en samenstelling bevat. Dat genetisch materiaal geven ze door aan hun nakomelingen. Een cruciaal kenmerk van levende cellen. Bovendien kan het genetisch materiaal van virussen mutaties (veranderingen) ondergaan, waardoor hun nakomelingen net iets andere eigenschappen kunnen krijgen. Virussen kunnen dus evolueren, ook zo’n basiskenmerk van alles wat leeft. En dan is er nog het gebruik van dezelfde bouwstenen. Voor leven zijn twee groepen bouwstenen essentieel: de nucleïnezuren en de aminozuren. Maar datzelfde geldt voor virussen.
Genetische parasieten
De nucleïnezuren zijn de ‘letters’ die samen het DNA en RNA, de dragers van de genetische informatie, vormen. Zowel levende cellen als virussen maken gebruiken van dezelfde letters. Ze spreken als het ware dezelfde taal. Je kunt aan een stukje DNA daarom niet meteen zien of het uit een levende cel of uit een virus komt. Dat verklaart ook waarom levende cellen geen enkel probleem hebben om virale genetische informatie te lezen en te verwerken. Of zelfs op te slaan en te gebruiken in hun eigen DNA.
De andere groep belangrijke bouwstenen zijn de aminozuren, waaruit alle eiwitten worden samengesteld. Eiwitten zijn de uitvoerders van zo’n beetje alle taken; ze zorgen voor transport, energieproductie, reparatie, opslag, afvalverwerking en nog veel meer. Eiwitten zijn lange strengen aan elkaar gekoppelde aminozuren die nauwkeurig tot ingewikkelde driedimensionale structuren zijn gevouwen. Er zijn twintig verschillende aminozuren beschikbaar in de natuur en alle levende cellen maken gebruik van die twintig. Virussen bevatten ook eiwitten, onder meer in hun omhulsel. Ook die eiwitten bestaan uit dezelfde twintig aminozuren. Net als bij het DNA kun je aan een eiwit niet meteen zien of het uit een virus of uit een cel komt.
Al met al levert dit een rare situatie op. We hebben dus twee soorten ‘dingen’ die uit exact dezelfde bouwstenen bestaan: cellen en virussen. De cellen leven, de virussen niet. Maar virussen als dood materiaal omschrijven zoals vaak gebeurt, klopt ook niet. Wat niet heeft geleefd, kan niet dood zijn. Virussen kunnen bovendien biologisch actief zijn en zich ‘levend’ gedragen, als ze zich nestelen in een gastheer. Dus virussen behoren ook niet tot de levenloze wereld, zoals de mineralen en het gesteente. Wat zijn het dan wel? Volgens Bas Dutilh, universitair docent bioinformatica aan de Universiteit Utrecht zijn het ‘genetische parasieten in een omhulsel van eiwitten’.
Kip of ei?
Met die omschrijving omzeil je meteen de vraag of het wel dan niet om leven gaat. Virussen zijn ‘gewoon’ verpakte stukjes genetisch materiaal die, zodra ze onderdak bij een gastheercel hebben gevonden, meeliften op de dagelijkse processen van de cel. Zoals het kopiëren van de virale genen, het in elkaar vouwen van de benodigde eiwitten en het vormen van nieuwe virusdeeltjes die vervolgens de cel verlaten en op zoek gaan naar een nieuwe gastheer. Dat virussen baat hebben bij deze strategie is overduidelijk, maar de vraag is hoe deze genetische parasieten ooit konden ontstaan.
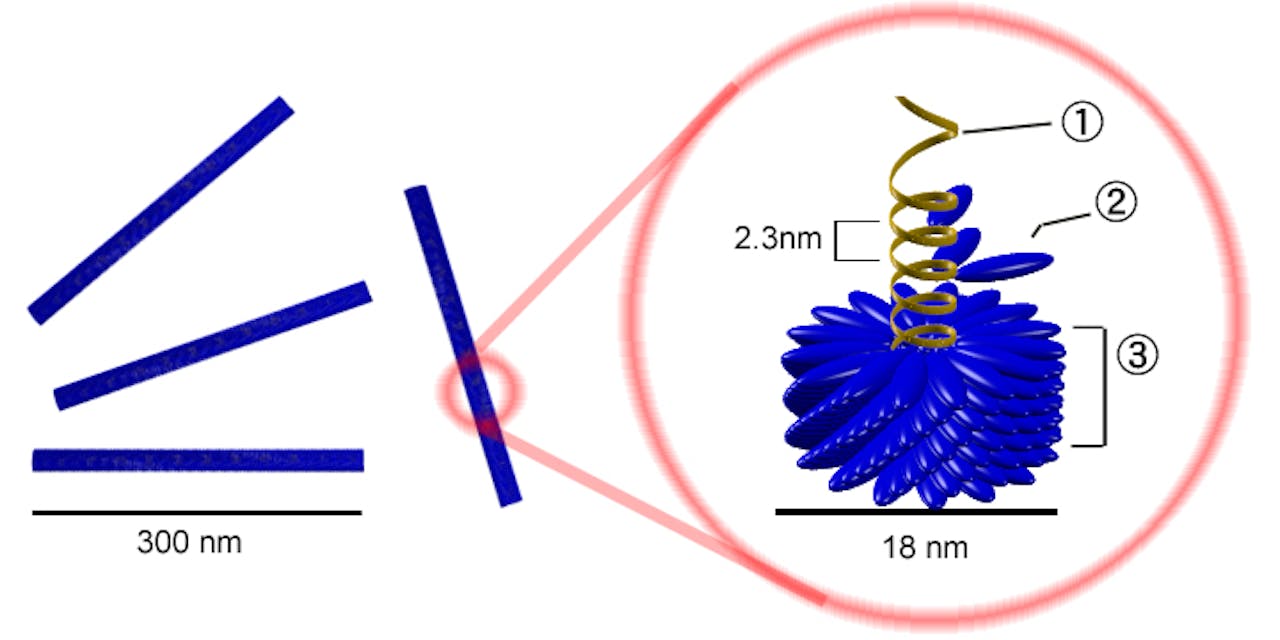
Opbouw van het Tobacco Mosaïc Virus, dat eind 19e eeuw werd ontdekt als eerste virus. Links de staafvormige virusdeeltjes, rechts een doorsnede. 1:RNA, 2: manteleiwit en 3: capside (het geheel van de manteleiwitten)
Y_tambe via Wikimedia Commons CC BY SA 3.0Een parasiet heeft een gastheer nodig, dus moeten er eerst cellen zijn gevormd, waarna de eerste virussen konden ontstaan. Dat is althans de visie van de zogeheten ‘cells first’-theorie. “Maar virussen hoeven niet als parasieten te zijn begonnen”, aldus Dutilh. “Dat is hoe we virussen nu definiëren. Maar dat wil niet zeggen dat het altijd zo was.” Terugredeneren vanuit de huidige situatie is riskant, vindt Dutilh, omdat onze blik beperkt is. Je mist dan de andere routes die gedurende de evolutie misschien zijn gevolgd, maar voor ons niet meer zichtbaar zijn.
De vraag naar de oorsprong van virussen lijkt sterk op de vraag naar de oorsprong van leven. Met dezelfde problemen. In beide gevallen weten we niet exact waar we naar zoeken, omdat we geen beeld hebben van hoe de voorlopers van de eerste cellen respectievelijk de eerste virussen en hun gastheren eruitzagen. Wat we wel weten is dat de wereld van de virussen ongelooflijk divers is. Alle levende cellen bevatten twee om elkaar gewikkelde strengen DNA – de bekende dubbele DNA-helix – met daarop de complete genetische code van die cel. Virussen gebruiken een veel breder repertoire voor de opslag van hun genen. Er zijn virussen die, net als cellen, dubbelstrengs DNA hebben, maar er zijn ook virussen met slechts één streng DNA of met alleen maar RNA, het ‘andere’ genetische molecuul. Dat RNA kan dan ook weer één streng zijn, of twee. En dan laten we verschillende manieren waarop die DNA of RNA strengen zijn opgeslagen en/of worden afgelezen hier nog even buiten beschouwing.
Gejatte eiwitten
Niet alleen de variatie wat betreft de genomen – het totale pakket aan genetisch materiaal – is groot, ook de manier waarop virussen te werk gaan varieert enorm. Bij een virus denken we meteen aan iets agressiefs dat zo snel en zoveel mogelijk cellen infecteert en vernietigt, maar dat geldt lang niet voor alle virussen. Dutilh: “Om goed na te kunnen denken over de oorsprong van virussen moeten we eigenlijk begrijpen hoe ze verwant zijn aan andere genetische parasieten.” Volgens hem zijn er verschillende niveaus van genetische parasieten. Hij somt op: “Ten eerste is er de kale genetische parasiet, een stukje genetisch materiaal dat zich ergens in kan nestelen en zich kan vermenigvuldigen. Maar dat kan buiten een gastheercel niet lang overleven. De tweede mogelijkheid zijn eenvoudige virussen, een combinatie van een genetische parasiet met een capside. Dat is de eiwitmantel die het genetisch materiaal omhult en zorgt voor bescherming. Een soort verpakking die transport mogelijk maakt. En dan zijn er ook nog zeer grote, complexe virussen die naast vermenigvuldiging en bescherming nog een heleboel extra eiwitten bevatten en mogelijk voor langere tijd een gastheercel overnemen. Die jumbo virussen zijn pas net ontdekt en geven een heel ander beeld van wat virussen allemaal kunnen.”
Deze indeling, waarbij de term virus een steeds complexer geheel beschrijft, wijst meteen op een vorm van evolutie. Virussen zijn aangetoond in alle levensvormen die we kennen, van de meest primitieve tot de meest moderne. Het is dus niet ondenkbaar dat virussen ook al heel vroeg tijdens de evolutie van het eerste leven zijn ontstaan. De eiwitten waarmee sommige virussen zich omhullen zijn behoorlijk ingewikkeld en lijken bovendien opvallend veel op de eiwitten die ook in levende cellen een rol spelen. Dat duidt erop dat virussen gaandeweg de evolutie op de een of andere manier aan die eiwitten zijn gekomen, dat er uitwisseling of gewoon ordinair jatwerk heeft plaatsgevonden. Dat laatste gebeurt heel veel, zegt Dutilh. “Capside-eiwitten zijn bijvoorbeeld vaak gejat van de gastheer. Nieuwe virussen ontstaan ook doordat stukjes genetisch materiaal elkaar ontmoeten in een gastheercel en zich nestelen in een capside van een oud virus. En zo heb je heel eenvoudig weer een nieuw virus.”
Replicatoren in de oersoep
Wil je zoeken naar de oorsprong van de virussen, dan lijkt het verstandig te kijken naar de kale genetische parasieten. Want dat is wat alle virussen gemeen hebben. De vraag is dus: waar komen die rondzwervende, losse genen of groepjes genen vandaan? Daarvoor zijn in de loop der jaren drie antwoorden geformuleerd: ‘virus early’, regressieve evolutie en ontsnapte genen. Bij ‘virus early’ is de aanname dat de eerste virussen tegelijk met de eerste cellen zijn ontstaan, vanuit dezelfde moleculen die in de figuurlijke oersoep beschikbaar waren. Er was ooit een plek waar de eerste stapjes richting leven zijn gezet en waar allerlei verschillende ‘replicatoren’, moleculen die zichzelf kunnen kopiëren zoals RNA, werden gevormd. Ook weten we dat de eerste aminozuren al beschikbaar waren in de oersoep. Uit al die replicatoren zijn zowel de voorlopers van de cellen ontstaan als de eerste genetische parasieten. Dat verklaart waarom cellen en virussen uit dezelfde bouwstenen bestaan: ze stammen uit dezelfde bron.
De benadering van de ‘regressieve evolutie’ beweert juist iets heel anders. Volgens deze verklaring zijn eerst de cellen ontstaan en is daarna op verschillende momenten een sterke versimpeling opgetreden. Cellen hadden bepaalde functies niet meer nodig en stootten daarom stukken DNA en eiwitten af, waardoor er een heel eenvoudig ‘aftreksel’ van de cel overbleef dat niet meer alles zelf kon en dus moest gaan parasiteren. Zie hier de oorsprong van de virussen. Maar deze uitleg heeft nog heel weinig aanhang, laat Dutilh weten. “Regressieve evolutie bestaat zeker, dat is het niet. We weten dat soorten gemakkelijk genen kunnen afstoten die ze niet gebruiken. Dit fenomeen, gene loss, is een bekende en belangrijke evolutionaire drijfveer. Maar als enige verklaring voor het ontstaan van virussen voldoet het niet.”
Tot slot zijn er nog de ‘ontsnapte genen’ als verklaring. Dit is zeker een realistische manier waarop nieuwe virussen kunnen ontstaan, zoals Dutilh eerder uitlegde over stukjes genetisch materiaal die een oud capside overnemen. Of een parasiet die eiwitten jat van de gastheer. Maar het kan niet alle variëteit in genen die we zien in virussen verklaren. Vergelijkend genetisch onderzoek kan lang niet voor al die genen een connectie maken met een gastheer waar dit gen uit ontsnapt zou kunnen zijn. Dutilh ziet het meest in een combinatie van de scenario’s. “Het is zeer waarschijnlijk dat de oorsprong van de virussen ligt in die gemeenschappelijk poel van bouwstenen waarin ook de basis voor de eerste cellen ligt. En daarna zijn er tal van mogelijkheden waarop steeds nieuwe en andere virussen konden ontstaan, onder meer via ontsnapte genen en misschien ook weleens via regressieve evolutie van complexe naar simpele virussen, en andersom.”
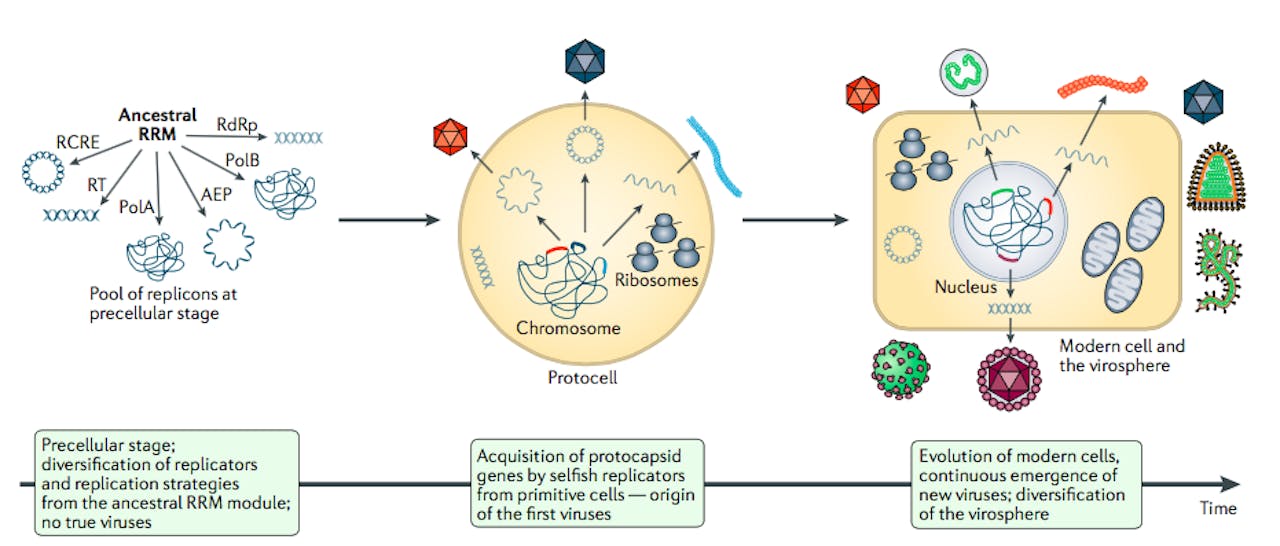
Een nieuwe benadering: virussen hebben een chimere oorsprong. Het genetisch materiaal is net zo oud als de voorlopers van de eerste cellen, maar later zijn de overige element zoals de capsiden ontstaan.
Krupovic, Dolja, Koonin, Nat Rev Microbiol (2019)Geen stamboom
Een sterke aanwijzing voor zo’n combinatie van scenario’s is dat er vooralsnog er geen enkel zicht is op een gemeenschappelijke voorouder van de virussen. Dutilh is ook lid van de International Committee on Taxonomy of Viruses, de club die over de naamgeving en indeling van de virussen gaat. “We zijn er wel uit dat we niet één overkoepelende stamboom van de virussen kunnen maken. Ze delen niets gemeenschappelijks, er is bijvoorbeeld geen gen of eiwit dat we in alle virussen terugvinden. Mocht er al een gedeelde voorouder zijn geweest, dan is die niet meer te vinden.” Waar het bij cellulaire organismen behoorlijk goed lukt om verwantschap aan te tonen door hun genomen te vergelijken, ligt dat bij virussen veel moeilijker. Dat komt onder meer doordat cellen veel energie steken in het intact houden van hun genoom en het repareren van foutjes. Virussen zijn veel minder precies. Aan controle en reparatie doen ze niet – daar hebben ze ook de mogelijkheid niet voor – en ze zijn niet kieskeurig. Stukken genetisch materiaal worden gemakkelijk uitgewisseld.
Bovendien ontstaan er veel verschillen tijdens hun verblijf in een gastheer. Bij het kopiëren van genen worden altijd foutjes gemaakt en als een virus een cel infecteert levert dat al snel honderden tot misschien wel duizenden nieuwe virusdeeltjes op. Dat geeft meteen heel veel variatie en al die virussen gaan weer andere cellen infecteren, met weer nieuwe kopieerfoutjes en zo krijg je heel snel een enorme variatie in genetisch materiaal. En een enorme hoeveelheid virussen die onderling ook net van elkaar kunnen verschillen. “De schatting is nu dat er 10 tot de macht 31 virussen en virus-achtige deeltjes zijn. Een tien met 31 nullen. En ze ontstaan constant, dus dat betekent dat zo’n beetje alle mogelijke genetische combinaties geprobeerd kunnen worden. Als een virus kan ontstaan zal het gebeuren.”
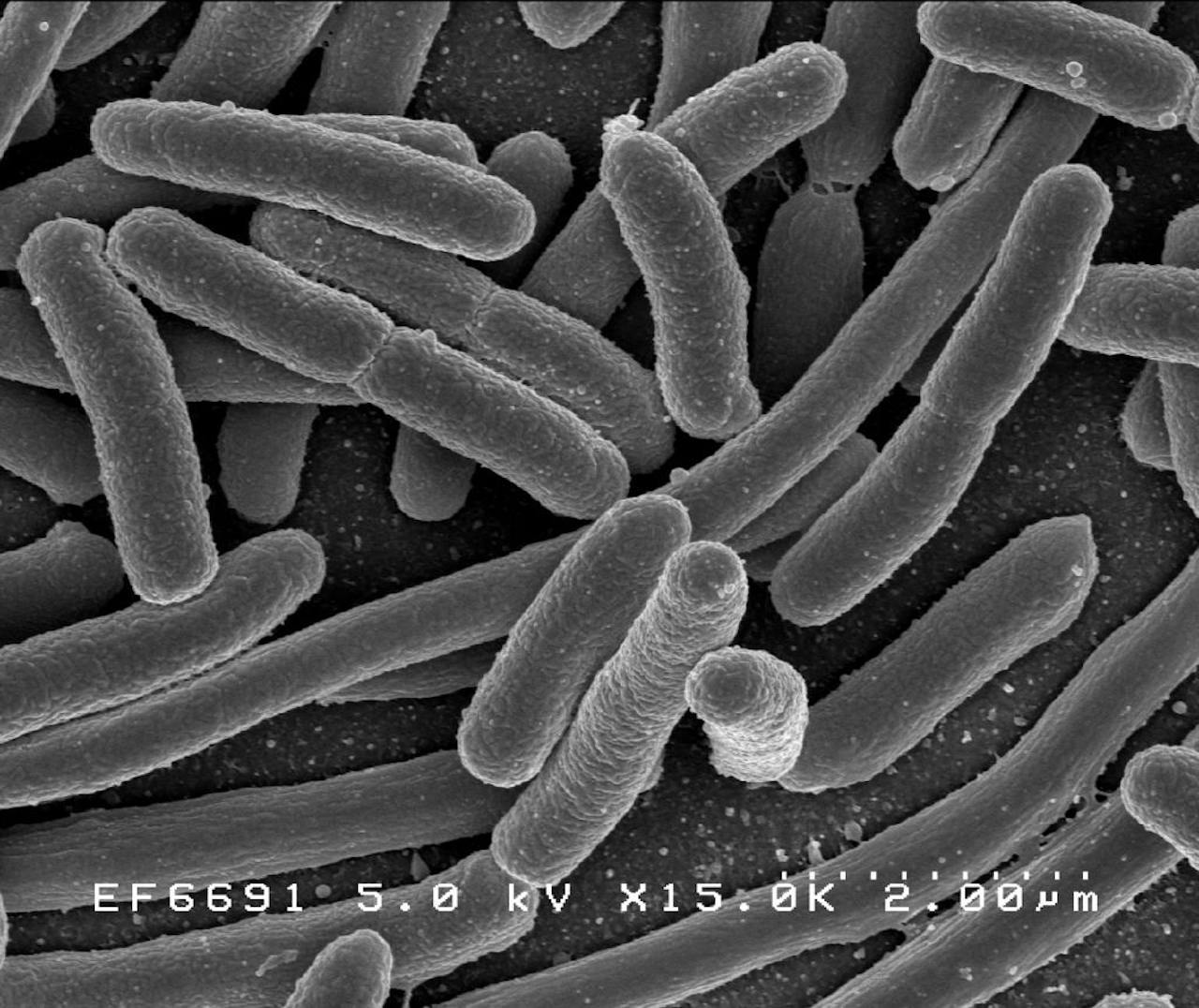
De bacterie E. coli is een bekende bewoner van het microbioom in de darmen. Een gezond microbioom bevat honderden verschillende soorten bacteriën. Bacteriofagen, de virussen die bacteriën infecteren, spelen een belangrijke rol bij het in stand houden van de biodiversiteit in de darmen.
NIAID via Wikimedia Commons, publiek domeinOmdat het kan
Dat klinkt deels best angstaanjagend, want er komt dus geen einde aan de stroom nieuwe virussen. Maar we zijn goed voorbereid, vindt Dutilh. Omdat al die virale variatie dus al zo oud is als het cellulaire leven hebben we tal van aanpassingen om ons tegen virussen te beschermen. Een snel veranderende vijand dwingt je tot flexibiliteit en aanpassing. “Dat staat bekend als de _Red Queen_-hypothese, vrij naar Alice in Wonderland. Beide partijen moeten even hard rennen om op dezelfde plek te blijven. Dat zien we in ecosystemen bij de co-evolutie van soorten, maar ook in de genetische opmaak van cellen die veel aan virussen zijn blootgesteld. De genen die coderen voor membraaneiwitten, dus de eiwitten die in contact staan met de omgeving, zijn het meest variabel. Die eiwitten staan doorlopend onder druk van virussen die willen binnendringen, dus de continue aanpassing en verandering is daar nodig om virussen te kunnen weerstaan.”
Is dat dan ook de rol van virussen in het grotere plaatje? Evolutie stimuleren? Is dat de verklaring dat ze (nog) bestaan? “Volgens Eugene Koonin, een van de toonaangevende onderzoekers in dit veld is het veel eenvoudiger. Genetische parasieten zijn gewoon onvermijdelijk. Ze kunnen ontstaan en dat gebeurt dus ook. Niet omdat het moet, maar omdat het kan”, zegt Dutilh. Dat wil niet zeggen dat virussen alleen maar nutteloze veroorzakers van ellende zijn, integendeel. Dutilh doet zelf veel onderzoek naar microbiomen, het stelsel van micro-organismen dat we vinden in de oceanen, in de bodem en ook in onze darmen. Voor hem horen de virussen daar integraal bij. “Wij hebben in het darmmicrobioom gekeken naar bacteriofagen, dat zijn virussen die bacteriën infecteren. Onze conclusie is dat de bacteriofagen hier zorgen voor biodiversiteit. Bacteriofagen houden snelgroeiende bacteriën onder controle. Als die uitgroeien, groeien de bacteriofagen mee en zorgen dus weer voor sterfte. Dat heet het ‘kill the winner’-effect en dat is belangrijk om te voorkomen dat een enkele soort bacterie de overhand krijgt. Goed nieuws voor ons, omdat een gezond darmmicrobioom gebaat is bij diversiteit.”
Overal virussen
Volgens Dutilh spelen virussen in het algemeen een belangrijke rol in het vormgeven van microbiële ecosystemen. “Als je dat soort systemen onderzoekt, waarbij je al het genetisch materiaal in bijvoorbeeld een bodem- of watermonster in kaart brengt, vind je overal viraal materiaal.” Maar hoe zie je dat genen uit een virus komen? De bouwstenen zijn immers gelijk. “Klopt, maar wat je met dit soort onderzoek altijd doet is vergelijken met de genomen waarvan de volgorde al bekend is. Dus je kijkt eerst of je een stukje kunt koppelen aan een virusgenoom dat we kennen. Als dat niet lukt, kijk je of je iets herkenbaars ziet in de databank van genomen uit cellulaire organismen. Levert dat nog niks op, dan zoek je naar stukjes die voor een eiwit coderen en dan probeer je uit de vinden of dat bekende eiwitten uit cellen of virussen zijn, daar zijn ook weer databanken voor. En als we echt geen enkele overeenkomst met een cellulair organisme vinden, is de voorlopige conclusie dat het uit een virus komt. Dat is omdat de cellulaire wereld veel beter beschreven is dan de virale wereld.”
Om onze kennis van de virosfeer en de evolutie van virussen een flinke boost te geven, pleit Dutilh, naast sequencing van virussen uit verschillende milieus, in eerste instantie voor grootschalig computationeel onderzoek, waarbij de volgorde van genomen wordt opgehelderd en vergeleken. “Veel data is al beschikbaar, maar we missen de mankracht en computers om alles goed te analyseren. We kennen nu het genoom van ongeveer 300 duizend cellulaire organismen tegenover minder dan 20 duizend virussen. Een groot verschil.” Meer kennis van de virale genen is volgens Dutilh de enige manier om uit te zoeken waar die genen vandaan komen en hoe de evolutie van virussen is verlopen.
Maar als we dat allemaal weten en we weten hoe virussen zijn ontstaan, zijn er dan Grote Vragen die we kunnen beantwoorden? “Dit is fundamenteel onderzoek en daarbij draait het erom dat je de mogelijkheid creëert voor toekomstige vragen om beantwoord, of zelfs gesteld te worden. We weten nog maar relatief kort dat virussen en ook de fagen bestaan, pas iets meer dan honderd jaar. Maar door die ontdekking van toen kunnen we nu vragen stellen over hoe ze werken en waar ze vandaan komen. Zo zal het blijven gaan.”
Terugkijken om te voorspellen
Toch ziet Dutilh ook meer tastbare toepassingen. “Bacteriofagen worden nu al toegepast als therapie. De ziekteverwekker wordt uit de patiënt geïsoleerd en geïnfecteerd met een faag om te zien of het werkt. Maar er zitten allerlei genen in die faag en je wilt eigenlijk van al die genen weten wat ze doen. Sommige fagen, zoals die van de cholerabacterie, maken namelijk gifstoffen aan ter bescherming van hun gastheer. Dat wil je toch wel vooraf weten, want een patiënt wil je niet blootstellen aan die gifstoffen.” Kennis van de genen in een faag geeft de mogelijkheid om te voorspellen wat er kan gebeuren. Tegelijkertijd vertelt het iets over de evolutie van die genen. “Je probeert te begrijpen hoe en waarom iets is ontstaan en wat de relatie is met verwante genen. Dat helpt bij voorspelling van genfuncties.” Terugkijken in de evolutie om een voorspelling te doen. Verder graven in de virosfeer kan ons dus veel leren over al het leven. Inclusief dat van ons.