Colloïdale deeltjes zijn overal. Je vindt ze in mist, rook, modder en melk. De industrie past ze toe bij de productie van elektronica, geneesmiddelen, verf en voedingsmiddelen. Colloïden kunnen zich als atomen en moleculen gedragen, maar zijn groot genoeg om makkelijk waar te nemen. Dit alles maakt ze tot interessante studieobjecten in wetenschappelijk onderzoek.

Melk bevat colloiden: vetdruppels en eiwitten in water.
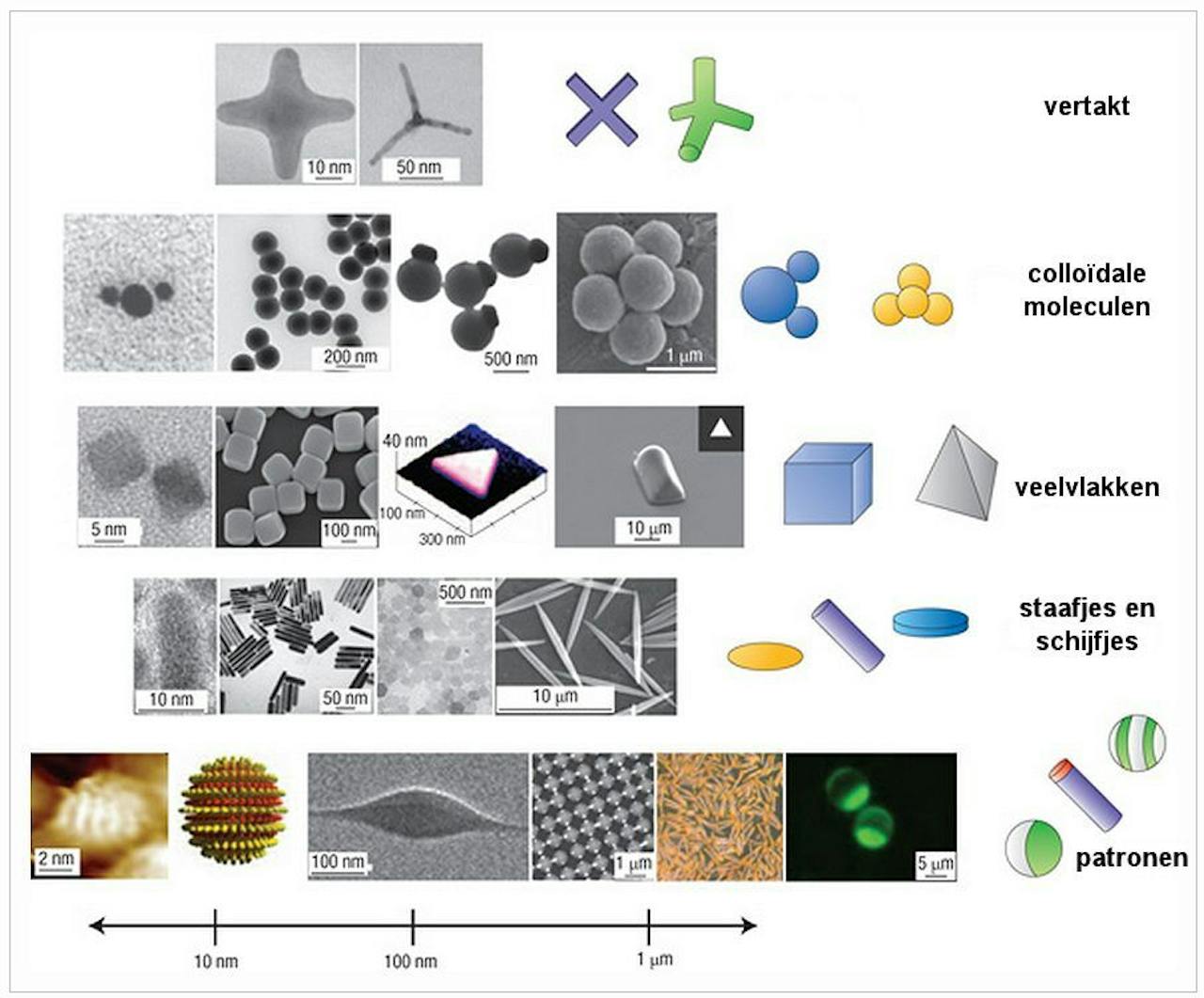
congerdesign, CC0 via PixabayMaar eerst: wat zijn colloïden precies? Eigenlijk is dat heel eenvoudig. Colloïden (of colloïdale deeltjes) zijn deeltjes met een afmeting tussen één en duizend nanometer. Nanodeeltjes dus. Ze zijn er in allerlei soorten. Je vindt ze bijvoorbeeld in mist (waterdruppels in de lucht), rook (roetdeeltjes in de lucht), modder (kleideeltjes in water), latexverf (oliedruppels in water), slagroom (luchtbellen in vet) en melk (vetdruppels en eiwitten in water).
In veel industriële processen spelen colloïdale systemen een cruciale rol. Daarom is het van belang ze in het laboratorium te onderzoeken. Een praktisch aspect is bijvoorbeeld het ‘uitzakken’ van het systeem. Dat gebeurt als de deeltjes na verloop van tijd samenklonteren en dus te groot worden om een colloid te zijn. Dit samenklonteren heet aggregatie, en in het geval van vloeibare deeltjes of gasbellen spreek je van samenvloeiing. Het is handig om te weten waar je op moet letten om deze verschijnselen te voorkomen.
Modelsysteem
Het interessante van colloïdale deeltjes is dat ze zich door hun afmeting op het grensgebied bevinden van twee werelden. Ze zijn zo klein dat ze zich als atomen en moleculen kunnen gedragen, maar groot genoeg om nog gezien te kunnen worden. Waar atomen en moleculen alleen met behulp van dure apparatuur ‘zichtbaar’ te maken zijn, kun je colloïden vaak al bestuderen met een eenvoudige microscoop.
Dit bijzondere gedrag van colloïdale deeltjes wordt duidelijk als je ze bijvoorbeeld aan water toevoegt. Dan zakken ze niet als zandkorrels naar de bodem, maar ze bewegen kris kras door elkaar – net als atomen en moleculen. Een colloïdale dispersie is zo een uitstekend modelsysteem voor de studie van het gedrag van atomen en moleculen.
http://youtu.be/ExOrLtrj-eI
Nieuwe toepassingen
Een derde reden voor onderzoek aan colloïdale systemen is dat je er nieuwe dingen mee kunt doen. Eigenlijk zijn er oneindig veel toepassingen te bedenken, van de elektronica tot de medische wereld en de voedingsmiddelindustrie. Zo is onlangs nog onderzoek gedaan aan een manier om ijzerzouten te ‘verpakken’ in colloïdale deeltjes. Daarmee zou je voedingsmiddelen van extra ijzer kunnen voorzien dat gemakkelijk door het lichaam is op te nemen.
Er wordt momenteel ook hard gewerkt aan colloïdale deeltjes die in staat zijn zelf nieuwe, grotere structuren te vormen. Dit heet zelf-assemblage. Een natuurlijk voorbeeld hiervan is opaal, een edelsteen die uit een stapeling van silica-colloïden bestaat. Die stapeling zorgt in opaal voor een specifieke interactie met licht, zodat de edelsteen de meest prachtige kleuren vertoont. Het idee is nu om zelf zo’n stapeling van colloïden te bepalen en op die manier de interactie met licht te beïnvloeden. Zo zijn misschien fotonische kristallen te maken, die licht van bepaalde golflengten niet – of juist wél – doorlaten.
Een andere toepassing ligt in de medische wereld. Dankzij vérgaande controle over het productieproces van colloïden zijn ingewikkelde deeltjes te maken, die bijvoorbeeld uit meerdere materialen bestaan. Een prachtige toepassing hiervoor is de targeted drug delivery of targeted imaging. Je kunt dan een medicijn of contrastmiddel verpakken in nanoschilletjes, en op die schilletjes bepaalde antilichamen plaatsen. Wanneer deze deeltjes in de bloedbaan ingespoten worden dan zullen ze alleen blijven plakken aan de cellen die specifiek zijn voor de antilichamen, bijvoorbeeld de cellen in een tumor.
Met een contrastmiddel in de schilletjes kan zo erg makkelijk gezocht worden naar de tumor: alleen de tumorcellen zullen oplichten in de scan. Met een medicijn zal dit middel zéér gericht naar de juiste plek gebracht worden. Op deze manier is er minder medicijn nodig, wat tot minder bijwerkingen zal leiden.