Een vreselijk cliché en waarschijnlijk ook de titel van je scheikundeboek op de middelbare school: chemie is overal. Maar het is reuzehandig als je een fiets wilt repareren!
Hoe afgezaagd het ook klinkt, het is natuurlijk wel waar dat chemie overal is. Alles is nu eenmaal opgebouwd uit moleculen. En dus is alles scheikunde. Ik probeer het al voorzichtig aan mijn zoontje (5) uit te leggen. Ik zeg dan dat water uit watermoleculen bestaat en een fiets uit fietsmoleculen. Dat is voorlopig ingewikkeld genoeg. Het is toch ook bijna niet voor te stellen dat alles (mensen ook!) uit een berg uiterst precies gerangschikte moleculen bestaat?

De fiets van Dowine
Dowine de Bruijn voor NEMO KennislinkSoorten moleculen
De volgende stap is om uit te leggen dat een fiets uit meerdere soorten moleculen bestaat. Het rubber van de fietsband is opgebouwd uit heel andere moleculen dan het ijzer van het frame, of het schuim in je zadel. Al die moleculen hebben verschillende eigenschappen. Daarom is de band elastisch, het frame sterk en het zadel lekker zacht. De verschillende materialen voelen dus anders aan, zijn sterk of juist slap, en reageren ook anders. Een fietsband brandt en stinkt verschrikkelijk als je ‘m in het vuur gooit (omdat er veel zwavel in zit), maar het ijzeren frame wordt hooguit roodgloeiend en wellicht wat buigbaar.
Dat de band, het frame en het zadel uit verschillende moleculen bestaan, is dus waarschijnlijk niet eens zo moeilijk te bevatten. De onderdelen lijken helemaal niet op elkaar. Maar ook onderdelen die wel veel op elkaar lijken, zoals de zadelpen en het frame, kunnen uit heel verschillende moleculen bestaan. Ouderwetse frames zijn namelijk vaak van ijzer gemaakt en een zadelpen vaak van aluminium. Allebei metaal, allebei sterk, maar ze reageren heel anders wanneer je er base (natronloog bijvoorbeeld) bij doet. Aluminium kan met de base reageren, maar ijzer niet. Dat komt door een redoxreactie. Kijk maar eens in BINAS tabel 48 naar de halfreacties van ijzer, aluminium en water in basisch milieu:
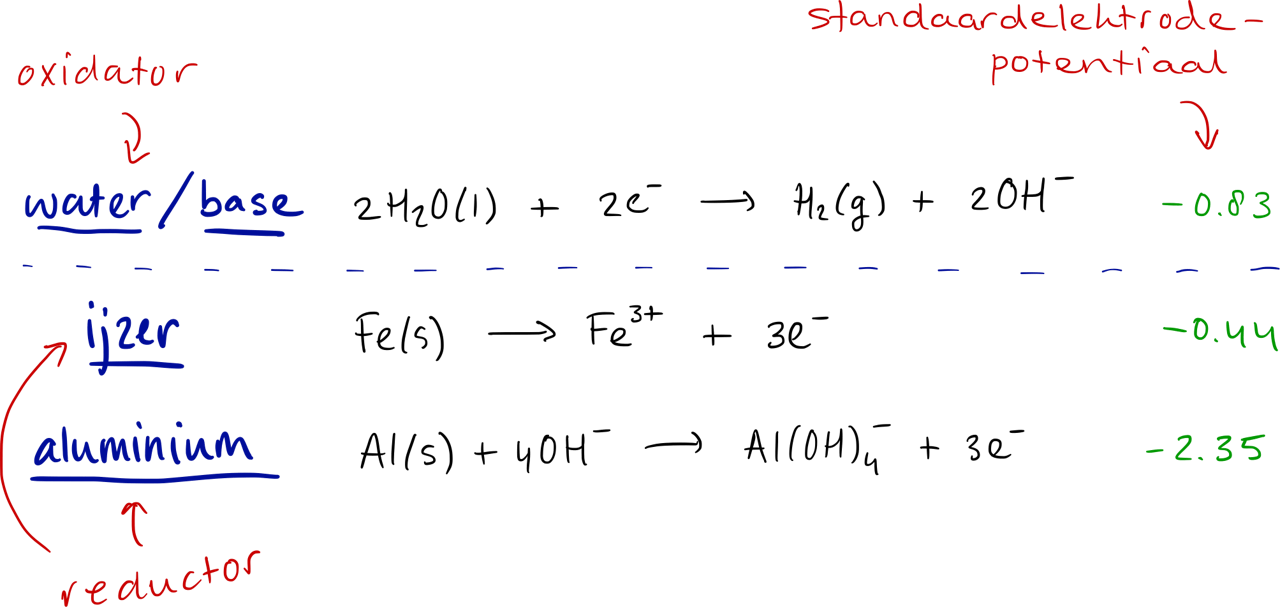
De halfreacties van ijzer, aluminium en water in basisch milieu (BINAS tabel 48)
Dowine de Bruijn voor NEMO KennislinkIn een redoxreactie worden elektronen (de e-) afgestaan door de reductor en opgenomen door de oxidator. Maar niet alle reductoren of oxidatoren zijn even sterk. Een redoxreactie kan daarom alleen optreden als de zogenaamde elektrodepotentiaal van de oxidator groter is dan die van de reductor. Die elektrodepotentiaal kan je meten, of opzoeken in BINAS. Aluminium en ijzer zijn beiden reductoren en moeten dus een lager potentiaal hebben dan de base waarmee ze zullen reageren. En daar zit ‘m precies het verschil.
De elektrodepotentiaal van ijzer is namelijk hoger dan dat van de base! Dus kan er geen redoxreactie plaatsvinden en gebeurt er niets wanneer je een stuk ijzer in een badje base legt. Maar de elektrodepotentiaal van aluminium ligt juist veel lager dan van de base. Aluminium reageert dus wél met base. In een badje base lost het aluminium daarom langzaam op in het water. Er komt daarbij ook waterstof vrij volgens de volgende vergelijking:

Zo, best zware kost voor een blog! Je vraagt je natuurlijk af waarom ik hierover schrijf. Wat maakt het nu uit of een metaal wel of niet met base kan reageren. Wat heb je daar nu aan in het dagelijks leven? Nou, door het verschil in reactiviteit van ijzer en aluminium, heb ik mijn fiets kunnen repareren! Er zat een aluminium zadelpen volledig vastgeroest in een ijzeren frame. Je kreeg het er met geen mogelijkheid meer uit en ik zou het frame eigenlijk weg moeten gooien. Maar met deze chemische aanpak, kon ik het aluminium letterlijk oplossen en zo de zadelpen eruit halen!
Toch wel handig dat chemie overal is! En ik kom nu ook weer overal op mijn gerepareerde fiets.
N.B. : natronloog is een gevaarlijke bijtende stof en waterstofgas is extreem brandbaar. Doe deze reactie dus liever niet na en liever niet thuis. Als je het wel doet, zorg dan voor goede bescherming (handschoenen, veiligheidsbril) en doe het buiten!

